Trophoblast funktioner, lag og udvikling
den trofoblasten er en struktur udgjort af et sæt celler, der danner det ydre lag, der omgiver en blastocyst, i tidlige stadier af den embryonale udvikling af pattedyr. Udtrykket kommer fra græsk trofos, hvilket betyder "feed" og af jeg blast, der henviser til den embryonale bakteriecelle.
Under de tidlige stadier af graviditeten af de plasentale pattedyr er trophoblastcellerne de første til at differentiere til en ægløsning, der er befrugtet. Dette sæt celler er kendt som trophoblast, men efter gastrulering kaldes de trophoectoderm.
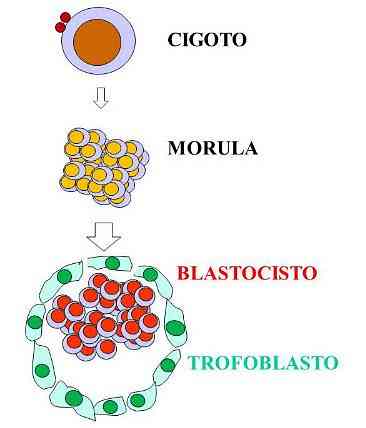
Trophoblast giver næringsstoffer til det udviklende embryo og letter dets implantation til livmoderen på grund af dets evne til at udrydde livmodervævets liv. Blastocysten kan således forbinde hulrummet dannet af livmodervæggen, hvor det vil absorbere næringsstoffer fra væsken fra moderen.
indeks
- 1 funktioner
- 2 lag
- 2.1 Sincitiotrophoblast
- 2.2 Citotrophoblast
- 3 udvikling
- 4 referencer
funktioner
Trofoblast spiller en afgørende rolle i implantation og placentation. Begge processer forekommer korrekt som en konsekvens af molekylær kommunikation mellem føtal og modervæv, medieret af hormoner og membranreceptorer.
Under implanteringen af blastocysten genereres nye typer af forskellige trofoblastiske celler, kaldet den villøse og ekstravilløse trofoblast. Den førstnævnte deltager i udvekslingen mellem fosteret og moderen, og sidstnævnte forbinder det placentale legeme til livmodervæggen.
På den anden side er placentationen præget af invasionen af livmoderpiralarterierne ved ekstravellosus trofoblastiske celler, der opstår ved forankringen af villi. På grund af denne invasion erstattes den arterielle struktur af amorffibrinoidmateriale og endovaskulære trofoblastiske celler..
Denne transformation etablerer et perfusionssystem med lav kapacitet og høj kapacitet fra de radiale arterier til det mellemrum, hvor det hårede træ er indlejret.
Graviditetens fysiologi afhænger af den ordnede udvikling af strukturelle og funktionelle ændringer af den villøse og ekstravilløse trofoblast.
Dette betyder, at en forstyrrelse af sådanne processer kan føre til forskellige former for komplikationer af forskellig grad af sværhedsgrad, herunder det mulige tab af graviditet og dødelige sygdomme.
Trofoblasten, selvom den ikke direkte bidrager til dannelsen af embryoet, er en forløber for moderkagen, hvis funktion er at etablere forbindelse med moderens livmoder for at tillade ernæringen af det udviklende embryo. Trofoblast er tydeligt fra dag 6 i humane embryoner.
lag
Under implantering vokser og multipler trofoblasten i to lag:
sincitiotrofoblasto
Syncytiotrophoblast er det yderste lag af trophoblast, dets celler har ikke intercellulære grænser, fordi deres membraner er gået tabt (syncytium). Af denne grund observeres cellerne som multinucleaterede og danner ledninger, der infiltrerer endometriumet..
Cellerne i syncytiotrophoblast kommer fra fusion af cellerne i cytotrophoblasten, og deres vækst forårsager dannelsen af chorioniske villi. Disse tjener til at forøge overfladen, der tillader strømmen af næringsstoffer fra moderen til fosteret.
Gennem apoptose (programmeret celledød) af livmoderstromcellerne skabes der rum, gennem hvilke blastocysten trænger mere ind i endometriumet.
Endelig produceres hormonet humant choriongonadotropin (HCG) i syncytiotrophoblast, som detekteres efter anden uge af graviditeten..
cytotrofoblast
For sin del udgør cytotrophoblast det inderste lag af trofoblastet. Dybest set er det et uregelmæssigt lag af ovoide celler med en enkelt kerne, og derfor kaldes de mononukleære celler.
Cytotrophoblast er direkte under syncytiotrophoblast, og dets udvikling begynder fra den første uge af svangerskabet. Trofoblast letter embryoimplantationen gennem cytotrophoblastceller, som har evnen til at differentiere i forskellige væv.
Den korrekte udvikling af cytotrophoblastceller er afgørende for den vellykkede implantation af embryoet til livmoderendometrium og er en stærkt reguleret proces. Den ukontrollerede vækst af disse celler kan imidlertid generere tumorer, såsom choriocarcinom..
udvikling
I den tredje uge omfatter processen med embryonal udvikling også den fortsatte udvikling af trofoblast. I første omgang dannes de primære villi af den interne cytotrophoblast omgivet af det ydre lag af syncytiotrophoblast.
Derefter migrerer cellerne i den embryonale mesoderm mod den primære villus-kerne, og dette sker i løbet af den tredje uge af svangerskabet. I slutningen af denne uge begynder disse mesodermale celler at singulere til dannelse af blodkarceller.
Da denne proces af celledifferentiering udvikler sig, vil det såkaldte hårvildt system danne sig. På dette tidspunkt dannes placentale villi, som vil være den endelige.
Kapillærerne, der dannes ud fra denne proces, kommer senere i kontakt med andre kapillærer, der danner samtidigt i mesodermen af chorionpladen og fikseringspediklen..
Disse nydannede skibe kommer i kontakt med dem i det intraembryoniske kredsløbssystem. Således, i det øjeblik, hvor hjertet begynder at slå (dette sker i den fjerde udviklingsuge), vil det vilde system være klar til at levere de ilt og næringsstoffer, der er nødvendige for dets vækst.
Fortsat med udviklingen trænger cytotrophoblast endnu mere i den syncytiotrophoblast, der dækker håret, indtil det når moderens endometrium. De kommer i kontakt med nogle hårede stilke og danner den ydre cytotrofoblastiske dækning.
Dette lag går rundt om trofoblasten og slutter helt fast i kororpladen til endometrisk væv i slutningen af den tredje uge (dage 19-20) af svangerskabet..
Mens chorionhulen er forstørret, er embryoen forankret til sin trofoblastiske dækning af fikseringspediklen, en ret snæver koblingsstruktur. Derefter bliver fikseringspediklen navlestrengen, som forbinder placenta med embryoet.
referencer
- Cross, J.C. (1996). Trofoblast funktion i normal og preeklamptisk graviditet. Foster- og modermedicinsk gennemgang, 8(02), 57.
- Lunghi, L., Ferretti, M.E., Medici, S., Biondi, C., & Vesce, F. (2007). Kontrol af menneskelig trofoblastfunktion. Reproduktiv Biologi og Endokrinologi, 5, 1-14.
- Pfeffer, P. L., & Pearton, D. J. (2012). Trophoblast udvikling. reproduktion, 143(3), 231-246.
- Red-Horse, K., Zhou, Y., Genbacev, O., Prakobphol, A., Foulk, R., McMaster, M. & Fisher, S. J. (2004). Trofoblast-differentiering under embryoimplantation og dannelse af moder-føtal-grænsefladen. Journal of Clinical Investigation, 114(6), 744-754.
- Screen, M., Dean, W., Cross, J.C., & Hemberger, M. (2008). Cathepsinproteaser har forskellige roller i trofoblastfunktion og vaskulær remodeling. Udvikling, 135(19), 3311-3320.
- Staun-Ram, E., & Shalev, E. (2005). Human trophoblast-funktion under implantationsprocessen. Reproduktiv Biologi og Endokrinologi, 3(Figur 2), 1-12.
- Velicky, P., Knöfler, M. & Pollheimer, J. (2016). Funktion og kontrol af humane invasive trofoblast subtyper: Intrinsic vs. moderkontrol. Celleadhæsion og migration, 10(1-2), 154-162.


