Vandelektrolyseprocedure, teknikker, hvad er det til, hjemmeeksperiment
den vandelektrolyse det er nedbrydning af vand i dets elementære komponenter ved anvendelse af en elektrisk strøm. Når man fortsætter, dannes hydrogen og molekylært oxygen på to inerte overflader, H2 og o2. Disse to overflader er bedre kendt ved navnene på elektroder.
Teoretisk set er volumenet af H2 dannet skal være dobbelt så meget som O2. Hvorfor? Fordi vandmolekylet har et H / O forhold svarende til 2, det vil sige to H for hvert oxygen. Dette forhold kontrolleres direkte med dets kemiske formel, H2O. Imidlertid påvirker mange eksperimentelle faktorer de opnåede mængder.

Hvis elektrolysen udføres inden i rør, der er nedsænket i vand (øverste billede), svarer vandkolonnen med lavere højde til brint, da der er en større mængde gas, der udøver tryk på væskens overflade. Bobler omgiver elektroderne og slutter at stige, når vandets damptryk udløber.
Bemærk, at rørene er adskilt fra hinanden på en sådan måde, at der er en lav migration af gasser fra den ene elektrode til den anden. Ved lave skalaer repræsenterer dette ikke en overhængende risiko; men ved industrielle skalaer er gasblandingen af H2 og o2 Det er meget farligt og eksplosivt.
Af denne grund er de elektrokemiske celler, hvor vandelektrolyse udføres, meget dyre; de har brug for et design og elementer, der sikrer, at gassen aldrig blandes, en rentabel strømforsyning, høje koncentrationer af elektrolytter, specielle elektroder (elektrokatalysatorer) og mekanismer til opbevaring af H2 produceret.
Elektrokatalysatorer repræsenterer friktion og samtidig vingerne for rentabiliteten af vandelektrolyse. Nogle består af oxider af ædle metaller, såsom platin og iridium, hvis priser er meget høje. Det er på dette tidspunkt især hvor forskere går sammen for at udvikle effektive, stabile og billige elektroder.
Årsagen til disse bestræbelser er at fremskynde dannelsen af O2, som er givet ved lavere hastigheder i forhold til H2. Dette aftager ved elektroden, hvor O'en dannes2 det medfører som en generel konsekvens anvendelsen af et potentielt meget større end nødvendigt (overpotentiale); hvad er det samme for lavere ydelse og højere omkostninger.
indeks
- 1 Reaktion af elektrolyse
- 1.1 Halvcelle reaktioner
- 2 Procedure
- 3 teknikker
- 3.1 Elektrolyse med alkalisk vand
- 3.2 Elektrolyse med polymerelektrolytisk membran
- 3.3 Elektrolyse med faste oxider
- 4 Hvad er brugen af vandelektrolyse??
- 4.1 Produktion af brint og dets anvendelser
- 4.2 Som en debugging metode
- 4.3 Som iltforsyning
- 5 Hjem eksperiment
- 5.1 Hjemsvariabler
- 6 referencer
Elektrolysereaktion
Elektrolysen af vand involverer mange komplekse aspekter. Men i almindelighed ligger dens grundlag i en simpel global reaktion:
2H2O (1) => 2H2(g) + O2(G)
Som observeret i ligningen indgriber to vandmolekyler: man må normalt reduceres eller få elektroner, mens den anden skal oxidere eller tabe elektroner.
H2 Det er et produkt af vandreduktion, fordi gevinsten af elektroner fremmer protonerne H+ kan være kovalent bundet, og oxygenet transformeres til OH-. Derfor er H2 forekommer ved katoden, hvilket er den elektrode, hvor reduktionen forekommer.
Mens O2 kommer fra oxidation af vand, fordi det mister de elektroner, der tillader det at binde til hydrogen, og frigiver følgelig protoner H+. Den O2 forekommer ved anoden, elektroden hvor oxidation forekommer og i modsætning til den anden elektrode er pH omkring anoden sur og ikke grundlæggende.
Halvcelle reaktioner
Ovenstående kan opsummeres med følgende kemiske ligninger for halvcelle-reaktioner:
2H2O + 2e- => H2 + 2OH- (Katode, grundlæggende)
2H2O => O2 + 4H+ + 4e- (Anode, syre)
Vand kan dog ikke tabe flere elektroner (4e-), hvoraf det andet vandmolekyle vinder ved katoden (2e-); Derfor skal den første ligning multipliceres med 2 og trækkes derefter fra med den anden ligning for at opnå netligningen:
2 (2H2O + 2e- => H2 + 2OH-)
2H2O => O2 + 4H+ + 4e-
6H2O => 2H2 + O2 + 4H+ + 4OH-
Men 4H+ og 4OH- de danner 4H2Eller så eliminerer disse fire af de seks H molekyler2Eller forlader to og resultatet er den globale reaktion, der netop er opstået.
Halvcelle-reaktionerne ændres med pH-værdierne, teknikkerne og har også potentielle reduktions- eller oxidationspotentialer, som bestemmer, hvor meget strøm der skal leveres, så at elektrolysen af vandet fortsætter spontant.
proces
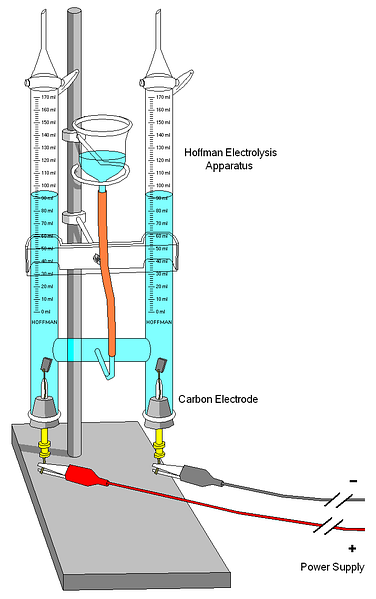
Det øverste billede viser et Hoffman voltmeter. Cylindrene er fyldt med vand og de valgte elektrolytter gennem den midterste dyse. Disse elektrolytteres rolle er at forøge vandets ledningsevne, fordi der under normale forhold er meget få H-ioner3O+ og OH- produkter af din auto ionisering.
De to elektroder er sædvanligvis platin, selv om de på billedet er erstattet af carbonelektroder. Begge er forbundet med et batteri, med hvilket en potentiel forskel (ΔV), som fremmer oxidation af vand (O-dannelse) påføres.2).
Elektronerne rejser hele kredsløbet, indtil du når den anden elektrode, hvor vandet vinder og bliver H2 og OH-. På dette tidspunkt er anoden og katoden allerede defineret, som kan differentieres af vandkolonnens højde; Den af mindre højde svarer til katoden, hvor H er dannet2.
I cylinderens øvre del er der nogle nøgler, der tillader frigivelse af de dannede gasser. Du kan nøje kontrollere H-tilstedeværelsen2 gør det reageret med en flamme, hvis forbrænding producerer gasformigt vand.
teknikker
Vandelektrolyteknikker varierer afhængigt af mængden af H2 og o2 der foreslås at generere. Begge gasser er meget farlige, hvis de blandes sammen, og derfor bærer de elektrolytiske celler komplekse konstruktioner for at minimere stigningen i gasformet tryk og deres diffusion gennem det vandige medium..
Også de teknikker varierer afhængigt af cellen, elektrolytten tilsættes til vandet, og elektroderne selv. På den anden side, nogle indebærer, at reaktionen udføres ved højere temperaturer, hvilket reducerer elforbrug og anden brug enormt pres for at holde H2 gemt.
Blandt alle teknikker kan følgende tre nævnes:
Elektrolyse med alkalisk vand
Elektrolysen udføres med basale opløsninger af alkalimetallerne (KOH eller NaOH). Med denne teknik forekommer reaktionerne:
4H2O (1) + 4e- => 2H2(g) + 4OH-(Aq)
4OH-(ac) => O2(g) + 2H2O (1) + 4e-
Som det kan ses, både ved katoden og ved anoden har vandet en basisk pH; og desuden OH- migrere til anoden, hvor de oxiderer til O2.
Elektrolyse med polymerelektrolytisk membran
Ved denne teknik anvendes en fast polymer, der tjener som en permeabel membran for H+, men vandtæt til gasser. Dette garanterer større sikkerhed under elektrolyse.
Halvcelle reaktionerne for denne sag er:
4H+(ac) + 4e- => 2H2(G)
2H2O (l) => O2(g) + 4H+(ac) + 4e-
Hionerne+ de vandrer fra anoden til katoden, hvor de bliver reduceret til at blive H2.
Elektrolyse med faste oxider
Meget forskellig fra de andre teknikker, der bruger oxider som elektrolytter, som ved høje temperaturer (600-900ºC) fungerer som et anion transportmedium.2-.
Reaktionerne er:
2H2O (g) + 4e- => 2H2(g) + 2O2-
2O2- => O2(g) + 4e-
Bemærk at denne gang er oxidanionerne, OR2-, dem, der rejser til anoden.
Hvad er brugen af vandelektrolyse?
Vandelektrolyse producerer H2 (g) og O2 (G). Ca. 5% af den producerede hydrogengas produceres ved elektrolyse af vand.
H2 det er et biprodukt af elektrolysen af vandige NaCl-opløsninger. Tilstedeværelsen af salt letter elektrolyse ved at øge vandets elektriske ledningsevne.
Den globale reaktion, der finder sted er:
2NaCl + 2H2O => Cl2 + H2 + 2 NaOH
For at forstå den enorme betydning af denne reaktion vil nogle af anvendelserne af gasformige produkter blive nævnt; fordi i dag er det dem der driver udviklingen af nye metoder til opnåelse af vandelektrolyse på en mere effektiv og grøn måde.
Af disse er de mest eftertragtede er at fungere som energi celler, som erstatter brugen af fossile brændstoffer afbrænding.
Produktion af brint og dets anvendelser
-Hydrogenet produceret i elektrolyse kan anvendes i kemiske reaktioner, der handler afhængighed, i hydrogeneringsprocesser, eller som et reduktionsmiddel i reduktionsprocesser.
-Det er også vigtigt i nogle handlinger kommerciel betydning, såsom: fremstilling af saltsyre, hydrogenperoxid, hydroxylaminer, etc. Involveret i syntesen af ammoniak ved en katalytisk reaktion med nitrogen.
-I kombination med ilt producerer det flammer med et højt kalorieindhold, med temperaturer på mellem 3.000 og 3.500 K. Disse temperaturer kan anvendes til skæringer og svejsninger i metalindustrien, til vækst af syntetiske krystaller, fremstilling af kvarts osv..
-Vandbehandling: Det for høje indhold af nitrater i vand kan reduceres ved eliminering i bioreaktorer, hvor bakterierne bruger hydrogen som energikilde
-Hydrogen går ind i syntesen af plast, polyester og nylon. Derudover er det en del af produktionen af glas, der øger forbrændingen under bagning.
-Reagerer med oxider og klorid af mange metaller, blandt dem: sølv, kobber, bly, vismut og kviksølv til fremstilling af rene metaller.
-Og derudover bruges den som brændstof i kromatografiske analyser med en flamme detektor.
Som en debugging metode
Elektrolysen af natriumchloridopløsninger anvendes til rensning af swimmingpoolvand. Under elektrolysen fremstilles hydrogen i katoden og chlor (Cl2) ved anoden. Der er tale om elektrolyse i dette tilfælde som saltchlorinator.
Klor opløses i vand, der danner hypochlorsyre og natriumhypochlorit. Hypochlorous syre og natriumhypochlorit steriliserer vand.
Som iltforsyning
Elektrolysen af vand bruges også til at generere ilt i den internationale rumstation, som tjener til at opretholde en iltatmosfære i stationen.
Hydrogen kan bruges i en brændselscelle, en metode til at opbevare energi og bruge det vand, der genereres i cellen til forbrug af astronauter.
Hjem eksperiment
Vandelektrolyseforsøg er blevet udført ved laboratorieskalaer med Hoffman voltmetre eller anden samling, der tillader at indeholde alle de nødvendige elementer i en elektrokemisk celle.
Af alle mulige samlinger og udstyr kan den enkleste være en stor gennemsigtig vandbeholder, som tjener som en celle. Derudover skal du også have en metal eller elektrisk ledende overflade til rådighed for at fungere som elektroder; den ene til katoden, og den anden for anoden.
Til dette formål kan selv blyanter med grafitpunkter, der skærpes i begge ender, være nyttige. Og endelig et lille batteri og nogle kabler, der forbinder det med de improviserede elektroder.
Hvis ikke gjort i en gennemsigtig beholder, kunne dannelsen af gasbobler ikke værdsættes.
Hjem variabler
Selvom elektrolyse af vand er et emne, der indeholder mange spændende og håbfulde aspekter for dem, der søger alternative energikilder, kan hjemmeforsøget være kedeligt for børn og andre tilskuere..
Derfor kan tilstrækkelig spænding påføres til dannelse af H-dannelse2 og o2 skifte visse variabler og notere ændringerne.
Den første er variationen i vandets pH ved at bruge enten eddike til at syrne vandet eller Na2CO3 at basere det lidt. En ændring i mængden af observerede bobler skal forekomme.
Derudover kunne det samme eksperiment gentages med koldt og varmt vand. På denne måde vil virkningen af temperatur på reaktionen blive overvejet.
Endelig, for at gøre dataindsamlingen lidt mindre farveløs, kan du ty til en meget fortyndet opløsning af lilla kåljuice. Denne saft er en basisk syreindikator af naturlig oprindelse.
Når det tilføjes til beholderen med de indførte elektroder, vil det bemærkes, at ved anoden bliver vandet lyserødt (surt), mens i katoden bliver farven gul (grundlæggende).
referencer
- Wikipedia. (2018). Elektrolyse af vand. Hentet fra: en.wikipedia.org
- Chaplin M. (16. november 2018). Elektrolyse af vand. Vandstruktur og videnskab. Hentet fra: 1.lsbu.ac.uk
- Energieffektivitet og vedvarende energi. (N.D.). Hydrogenproduktion: elektrolyse. Hentet fra: energy.gov
- Phys.org. (14. februar 2018). Høj effektivitet, lavpris katalysator til vandelektrolyse. Hentet fra: phys.org
- Kemi LibreTexts. (18. juni 2015). Elektrolyse af vand. Hentet fra: chem.libretexts.org
- Xiang C., M. Papadantonakisab K., og S. Lewis N. (2016). Principper og implementeringer af elektrolysesystemer til vanddeling. The Royal Society of Chemistry.
- Regents af University of Minnesota. (2018). Elektrolyse af vand 2. University of Minnesota. Hentet fra: chem.umn.edu


