Kemisk aktiveringsenergi, hvad den består af, beregning
den kemisk aktiveringsenergi (set ud fra kinetiske undersøgelser) henviser til den mindst mulige mængde energi, der kræves for at starte en kemisk reaktion. Ifølge teorien om kollisioner i kemisk kinetik siges det, at alle molekyler, der er i bevægelse, har en vis mængde kinetisk energi.
Det betyder, at jo større hastigheden af din bevægelse er, desto større er din kinetiske energis størrelse. I den forstand kan et molekyle, der bærer en hurtig bevægelse ikke opdeles i fragmenter alene, så der skal ske en kollision mellem dette og andet molekyle for en kemisk reaktion kan forekomme.
Når det sker - når der opstår en sammenstød mellem molekylerne - bliver en brøkdel af sin kinetiske energi omdannet til vibrationsenergi. Ligeledes, hvis den kinetiske energi ved starten af processen er høj, vil de molekyler, der deltager i kollisionen, fremvise en vibration så stor, at nogle af de kemiske bindinger, der er til stede, vil blive brudt..
Denne sammenbrud af koblinger er det første trin i omdannelsen af reaktanter til produkter; det vil sige i dannelsen af disse. Hvis derimod i starten af denne proces den kinetiske energi er af ringe størrelse, vil der være et fænomen af "rebound" af molekylerne, hvorigennem de vil adskille praktisk talt intakt..
indeks
- 1 Hvad består den af??
- 1.1 Aktiveret kompleks
- 2 Hvordan beregnes det?
- 2.1 Beregning af aktiveringsenergien af en kemisk reaktion
- 3 Hvordan påvirker aktiveringsenergien reaktionshastigheden?
- 4 Eksempler på beregning af aktiveringsenergi
- 5 referencer
Hvad består det af??
Ud fra konceptet mellem kollisioner mellem molekyler for at igangsætte de ovenfor beskrevne kemiske reaktioner kan man sige, at der er en minimumsmængde energi, der kræves for at en kollision kan opstå.
Så hvis energiindholdet er lavere end det krævede minimum, vil simpelthen ikke være nogen ændring mellem molekyler efter indgivelsen af kollisionen, hvilket betyder, at når denne energi er fraværende, de involverede arter forbliver stort set intakt og vil ikke ske enhver ændring som følge af dette chok.
I denne rækkefølge kaldes den mindste energi, der er nødvendig for en ændring, der opstår efter en kollision mellem molekyler, aktiveringsenergi.
Med andre ord skal molekylerne involveret i et chok have en mængde af den samlede kinetiske energi med en størrelse lig med eller større end aktiveringsenergien, således at en kemisk reaktion kan forekomme.
Også i mange tilfælde kolliderer molekylerne og opstår en ny art kaldet aktiveret kompleks, struktur som også kaldes "overgangsstatus", fordi den kun eksisterer midlertidigt.
Det skyldes reaktantartene som følge af kollisionen og forud for dannelsen af reaktionsprodukterne.
Aktiveret kompleks
Det ovennævnte aktiverede kompleks udgør en art, der har meget lav stabilitet, men som igen har en stor mængde potentiel energi.
Følgende diagram viser omdannelsen af reaktanter til produkter, udtrykt som energi og bemærke, at størrelsen af den energi aktiverede dannede kompleks er betydeligt højere end de observeres reaktanter og produkter.
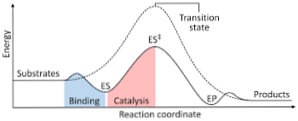
Hvis produkterne i slutningen af reaktionen har en større stabilitet end reaktantstofferne, forekommer frigivelsen af energi i form af varme, hvilket giver en eksoterm reaktion..
Omvendt, hvis reaktanterne er en stabilitet med større størrelse end produkterne, betyder det, at reaktionsblandingen viser en energiabsorption som varme fra sine omgivelser, hvilket resulterer endoterme reaktion typen.
Ligeledes skal der udformes et diagram, hvis den ene eller den anden forekommer, som den, der tidligere er vist, hvor den potentielle energi i systemet, som reagerer mod fremskridtet eller fremskridtet af reaktionen, er tegnet..
På den måde opnås de potentielle energiændringer, der sker, når reaktionen går videre, og reaktanterne omdannes til produkter.
Hvordan beregnes det?
Aktiveringsenergien af en kemisk reaktion er nært beslægtet med hastighedskonstanten for denne reaktion, og afhængigheden af denne konstant med hensyn til temperatur, er repræsenteret ved Arrhenius-ligningen:
k = ae-Ea / RT
I dette udtryk k repræsenterer reaktionens hastighedskonstant (som afhænger af temperaturen) og parameteren En det hedder frekvensfaktor, og det er et mål for hyppigheden af intermolekyl kollisioner.
For sin del, og udtrykker grundlaget for serien af naturlige logaritmer. Det hæves til en effekt svarende til aktiveringsenergiens negative kvote (Ea) mellem produktet resulterende fra gaskonstanten (R) og den absolutte temperatur (T) af systemet til at overveje.
Det skal bemærkes, at frekvensfaktoren kan betragtes som en konstant i visse reaktionssystemer over et bredt temperaturområde.
Denne matematiske udtryk blev påstået i første omgang af den hollandske-fødte kemiker Jacobus Henricus van't Hoff i 1884, men som gav videnskabelig validitet og fortolket sin forudsætning var den svenske kemiker Svante Arrhenius oprindelse, i 1889.
Beregning af aktiveringsenergien af en kemisk reaktion
Arrhenius-ligningen peger på den direkte proportionalitet, der eksisterer mellem hastighedskonstanten for en reaktion og hyppigheden af sammenstød mellem molekyler.
Også denne ligning kan repræsenteres på en mere bekvem måde ved at anvende egenskaben af naturlige logaritmer til hver side af ligningen, idet man opnår:
ln k = ln A - Ea / RT
Når man omordner betingelserne for at opnå ligningen af en linje (y = mx + b), opnås følgende udtryk:
ln k = (- Ea / R) (1 / T) + ln A
Så når konstruere en afbildning af ln k mod 1 / T en lige linje, hvor ln k opnås repræsenterer y-koordinaten, (-Ea / R) repræsenterer hældningen af linien (m), (1 / T) repræsenterer koordinaten x, og ln A repræsenterer skæringspunktet med koordinatets akse (b).
Som det kan ses, er hældningen som følge af denne beregning lig med værdien af -Ea / R. Dette indebærer, at hvis det ønskes at opnå værdien af aktiveringsenergien ved hjælp af dette udtryk, skal en simpel clearing udføres, hvilket resulterer i:
Ea = -mR
Her ved vi værdien af m og R er en konstant lig med 8.314 J / K · mol.
Hvordan påvirker aktiveringsenergien reaktionshastigheden?
Når man forsøger at lave et billede af aktiveringsenergien, kan det betragtes som en barriere, der ikke tillader en reaktion mellem de lavere energimolekyler.
Som i en fælles reaktion sker, at antallet af molekyler, der kan reagere, er ret stort, kan hastigheden - og ækvivalent den kinetiske energi af disse molekyler - være meget variabel.
Det sker som regel, at kun en lille del af totaliteten af de molekyler, der oplever en kollision - dem der har større bevægelseshastighed - præsenterer nok kinetisk energi for at kunne overvinde størrelsen af aktiveringsenergien. Så disse molekyler er egnede og kan være en del af reaktionen.
Ifølge Arrhenius-ligningen, den negative tegn, der går forud for forholdet mellem aktiveringsenergien og produktet af gassen konstant ved den absolutte temperatur indebærer, at hastighedskonstanten faldende gaver med en stigning i aktiveringsenergi, såvel som en vækst, når temperaturen stiger.
Eksempler på beregning af aktiveringsenergi
For at beregne aktiveringsenergien ved at konstruere en graf ifølge Arrhenius-ligningen, har vi, at hastighedskonstanterne for decetaleringsreaktionen af acetaldehyd er målt ved fem forskellige temperaturer, og vi vil bestemme aktiveringsenergien til reaktionen, som udtrykkes som:
CH3CHO (g) → CH4(g) + CO (g)
Dataene for de fem målinger er følgende:
k (1 / M1/2· S): 0,011 - 0,035 - 0,105 - 0,343 - 0,789
T (K): 700 - 730 - 760 - 790 - 810
For det første at løse dette mysterium og bestemme aktiveringsenergien er at opbygge en afbildning af ln k vs 1 / T (y vs x) for at opnå en lige linje og herfra tage hældningen og finde værdien af Ea, som forklaret.
Transformerende måledata ifølge Arrhenius-ligningen [ln k = (- Ea / R) (1 / T) + ln A] følgende værdier for y og x henholdsvis er:
ln k: (-4,51) - (-3,35) - (-2,254) - (-1,070) - (-0,237)
1 / T (K-1): 1,43 * 10-3 - 1,37 * 10-3 - 1,32 * 10-3 - 1,27 * 10-3 - 1,23 * 10-3
Af disse værdier og ved hjælp af matematisk beregning af hældningen - enten i en computer eller i en regnemaskine, ved hjælp af udtrykket m = (Y2-og1) / (X2-X1) eller ved hjælp af den lineære regressionsmetode - opnår vi det m = -Ea / R = -2.09 * 104 K. Så:
Ea = (8,314 J / K · mol) (2,09 * 104 K)
= 1,74 * 105 = 1,74 * 102 kJ / mol
For at bestemme andre aktiveringsaktiver ved hjælp af den grafiske måde udføres en lignende procedure.
referencer
- Wikipedia. (N.D.). Aktiveringsenergi. Hentet fra en.wikipedia.org
- Chang, R. (2007). Kemi, niende udgave. Mexico: McGraw-Hill.
- Britannica, E. (s.f.). Aktiveringsenergi. Hentet fra britannica.com
- Moore, J.W. og Pearson, R.G. (1961). Kinetik og mekanisme. Hentet fra books.google.co.ve
- Kaesche, H. (2003). Korrosion af metaller: Fysisk-kemiske principper og aktuelle problemer. Hentet fra books.google.co.ve


