Kemisk hybridisering sp, sp2, sp3
den kemisk hybridisering Det er "mix" af de atomorbitaler, hvis koncept blev indført ved kemiker Linus Pauling i 1931 for at dække skønhedsfejl valensbinding teori (TEV). Hvilke ufuldkommenheder? Disse er: molekylære geometrier og ækvivalente bindelængder i molekyler som methan (CH4).
Ifølge TEV i methan atomorbitaler af C formular fire obligationer o fire atomer H. 2p orbitaler, med former af ∞ (nederst) af C er vinkelrette på hinanden, således at H bør være adskilt fra hver af andre i en 90º vinkel.
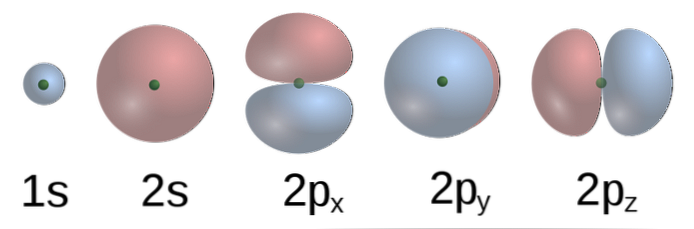
Derudover 2s orbital (sfærisk) binder til C 1s orbital H i en vinkel på 135 ° i forhold til de tre andre H. imidlertid eksperimentelt vist sig, at vinkler i CH4 er 109,5º, og at længderne af C-H-bindingerne desuden er ækvivalente.
For at forklare dette, skal en kombination af de originale atomorbitaler anses for at danne fire degenererede hybrid orbitaler (af lige energi). Her kommer kemisk kemi. Hvad er hybrid orbitaler? Det afhænger af atomorbitalerne, der genererer dem. De udviser også en blanding af disse elektroniske egenskaber.
indeks
- 1 sp3 hybridisering
- 1.1 Fortolkning
- 1.2 Afvigelser af vinklerne af links
- 2 Hybridisering sp2
- 3 Hybridisering sp
- 4 referencer
Hybridisering sp3
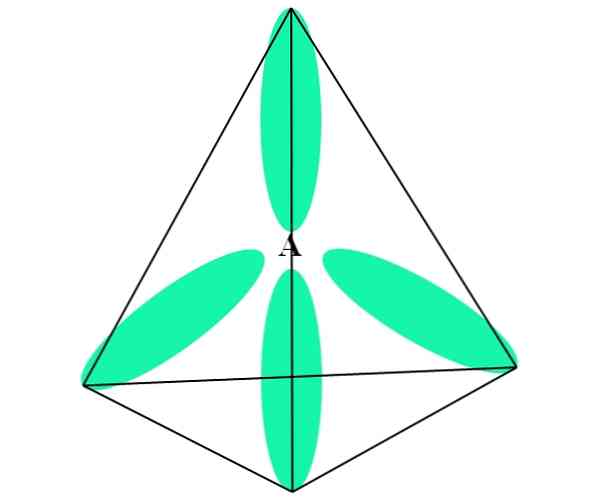
I tilfælde af CH4, Hybridisering af C er sp3. Fra denne tilgang er molekylær geometrien forklaret med fire sp orbitaler3 adskilt ved 109,5º og peger mod en tetraederens hjørner.
I billedet ovenfor kan du se hvordan sp orbitalerne3 (grøn) etablerer et tetrahedralt elektronisk miljø omkring atomet (A, som er C for CH4).
Hvorfor 109,5º og ikke andre vinkler, for at "tegne" en anden geometri? Årsagen er, at denne vinkel minimerer de elektroniske frastødninger af de fire atomer, der er forbundet med A.
På denne måde er CH-molekylet4 kan repræsenteres som en tetraeder (tetrahedral molekylær geometri).
Hvis der i stedet for H, C dannedes forbindelser med andre atomer, hvad ville det da være hybridiseringen? Så længe carbonet danner fire σ bindinger (C-A), vil dets hybridisering være3.
Det kan antages, at i andre organiske forbindelser, såsom CH3OH, CCl4, C (CH3)4, C6H12 (cyclohexan) osv., carbonet har en sp hybridisering3.
Dette er grundlæggende for at skitsere organiske strukturer, hvor carbon med simple bindinger repræsenterer divergenspunkter; det vil sige, at strukturen ikke forbliver i et enkelt plan.
fortolkning
Hvad er den enkleste fortolkning for disse hybrid orbitaler uden at adressere de matematiske aspekter (bølgefunktionerne)? Sp orbitals3 betyder, at de stammede fra fire orbitaler: en s og tre s.
Fordi kombinationen af disse atomorbitaler skal være ideel, de fire sp orbitaler3 resulterende er identiske og besidder forskellige retninger i rummet (såsom i orbitalerne px, pog og sz).
Dette gælder for andre mulige hybridiseringer: antallet af hybridorbitaler formular er den samme som den for de atomorbitaler kombineres. For eksempel sp hybrid orbitaler3d2 de er dannet af seks atomorbitaler: en s, tre p og to d.
Afvigelser af vinklerne af links
Ifølge teorien om elektronpar frastødning Layer Valencia (VSEPR), et par af frie elektroner optager mere volumen end et atom bundet. Dette får linkene til at bevæge sig fra hinanden, reducere den elektroniske spænding og aflede 109.5º vinklerne:
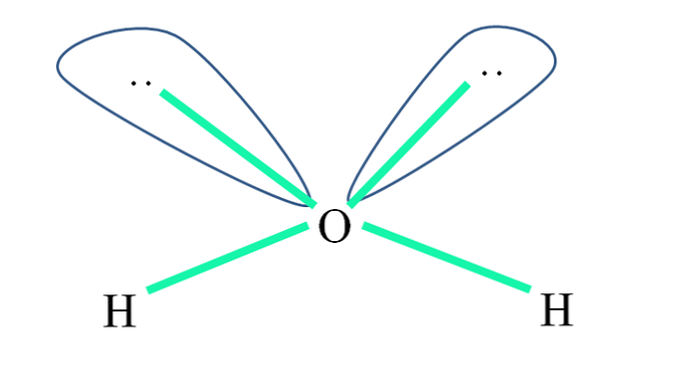
For eksempel er H-atomer i vandmolekylet bundet til sp orbitalerne3 (i grønt), og også de elektronpar, der ikke deles ":" optager disse orbitaler.
Frastødninger af disse par af elektroner er sædvanligvis repræsenteret som "to balloner med øjne", som på grund af deres volumen, Myggemidler to links o O-H.
Således i vandet er vinklerne af links virkelig 105º, i stedet for de 109,5º, der forventes for den tetrahedrale geometri.
Hvilken geometri har H da?2O? Den har en vinkelgeometri. Hvorfor? Fordi selv om den elektroniske geometri er tetrahedral, forringer to par ikke-delte elektroner den til en vinkelmolekylær geometri.
Hybridisering sp2
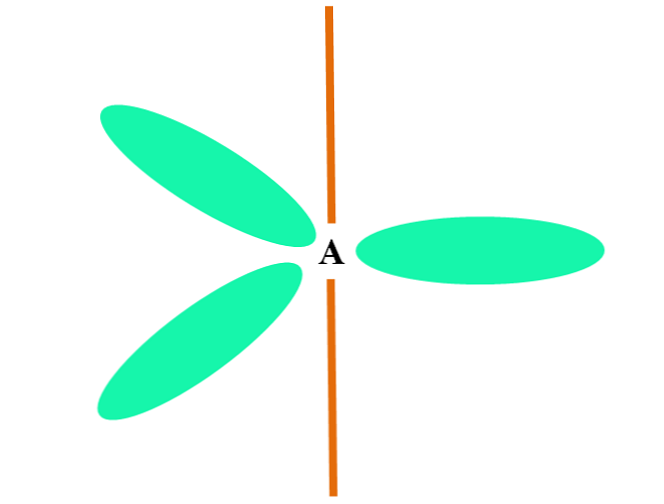
Når et atom kombinerer to p og en s orbitaler, genererer det tre sp hybrid orbitaler2; Imidlertid forbliver en orbital p uændret (fordi de er tre), som er repræsenteret som en orange stang i billedet ovenfor.
Her er de tre sp orbitaler2 de er grønne for at fremhæve deres forskel fra den orange bar: den "rene" p orbitale.
Et atom med sp hybridisering2 kan visualiseres som en flad trigonal gulv (trekanten trækkes med sp orbitals2 af grøn farve) med sine hjørner adskilt af 120º vinkel og vinkelret på en bar.
Og hvilken rolle spiller den rene p orbitale? Det at danne en dobbeltbinding (=). Sp orbitals2 tillade dannelsen af tre σ bindinger, mens den rene p orbitale a π binding (en dobbelt eller tredobbelt binding betyder en eller to π bindinger).
For eksempel at trække carbonylgruppen og strukturen af formaldehydmolekylet (H2C = O), fortsætter som følger:
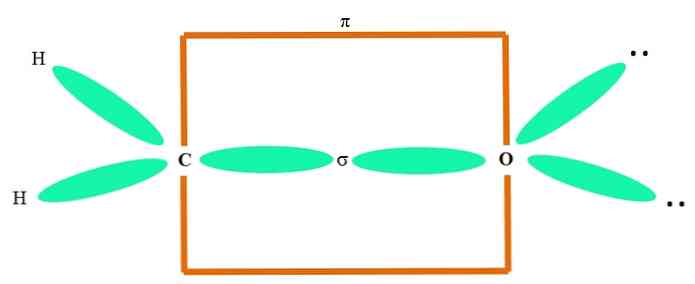
Sp orbitals2 både C og O danner en binding σ, mens deres rene orbitaler danner en binding π (det orange rektangel).
Det kan ses, hvordan resten af de elektroniske grupper (atomer H og ikke-fælles elektronpar) er placeret på andre orbitaler sp2, adskilt af 120º.
Hybridisering sp
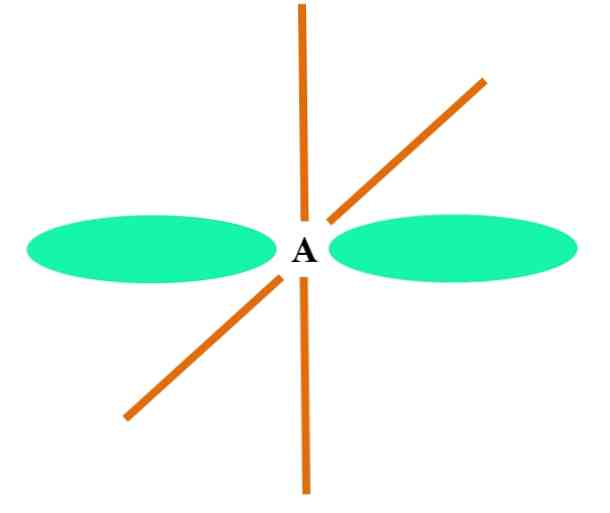
Det øverste billede viser et atom A med sp hybridisering. Her kombineres et orbital s og en p orbital med to degenererede sp orbitaler. Men nu forbliver to rene p-orbitaler uændrede, hvilket tillader A at danne to dobbeltbindinger eller en tredobbeltbinding (≡).
Med andre ord: hvis en struktur opfylder ovennævnte C (= C = eller = C), derefter hybridisering er sp. For andre mindre illustrerende ligesom transition- metaller atomer beskrivelse af elektroniske og molekylære geometrier betragtes også kompliceret, fordi d- orbitaler og til f.
Hybride orbitaler adskilles med en vinkel på 180º. Af denne årsag arrangeres de koblede atomer i en lineær molekylær geometri (B-A-B). Endelig, i billedet nedenfor kan du se strukturen af cyanidanionen:

referencer
- Sven. (3. juni 2006). S-p-orbitaler. [Figur]. Hentet den 24. maj 2018, fra: commons.wikimedia.org
- Richard C. Banks. (Maj 2002). Bonding og hybridisering. Hentet den 24. maj 2018, fra: chemistry.boisestate.edu
- James. (2018). En hybridiseringsgenvej. Hentet den 24. maj 2018, fra: masterorganicchemistry.com
- Dr. Ian Hunt. Department of Chemistry, University of Calgary. sp3 hybridisering. Hentet den 24. maj 2018, fra: chem.ucalgary.ca
- Kemisk binding II: Molekylær geometri og hybridisering af atomomridser Kapitel 10. [PDF]. Hentet den 24. maj 2018, fra: wou.edu
- Quimitube. (2015). Kovalent binding: Introduktion til hybridisering af atomorbitaler. Hentet den 24. maj 2018, fra: quimitube.com
- Shiver & Atkins. (2008). Uorganisk kemi (Fjerde udgave, side 51). Mc Graw Hill.


