Law of Boyle-Mariotte historie, matematisk udtryk, eksempler
Lovgivningen i Boyle er det der udtrykker forholdet mellem det tryk, der udøves af eller på en gas, og det volumen der er besat af det; holde konstant temperaturen af gassen såvel som dens mængde (antal mol).
Denne lov sammen med Charles, Gay-Lussac, Charles og Avogadro beskriver den opførsel af en ideel gas; specifikt i en lukket beholder underkastet volumenændringer udøvet af en mekanisk kraft.
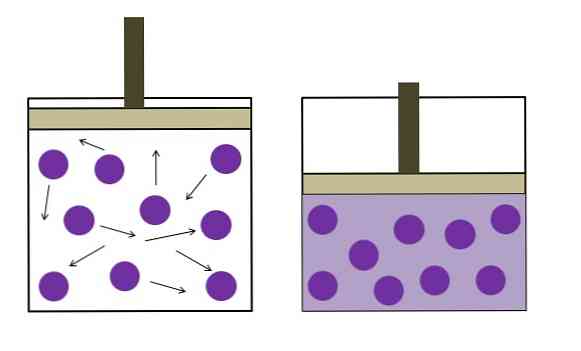
Billedet ovenfor kort opsummerer Boyle-Mariotte-loven.
De lilla prikker repræsenterer molekyler eller gasatomer, der kolliderer med beholderens indre vægge (til venstre). Ved at reducere den ledige plads eller volumen af beholderen, der optages af denne gas, stiger kollisionerne, hvilket betyder en stigning i tryk (højre).
Dette viser, at trykket P og volumen V af gassen er omvendt proportionelle, hvis beholderen er hermetisk forseglet; ellers ville et højere tryk svare til en større udvidelse af beholderen.
Hvis en plot V blev lavet mod P, med dataene henholdsvis V og P på henholdsvis Y og X-akserne, ville en asymptotisk kurve blive observeret. Jo mindre er V, desto større er stigningen i P; det vil sige, at kurven strækker sig til høje værdier af P på X-aksen.
Selvfølgelig forbliver temperaturen konstant; men hvis det samme eksperiment blev udført ved forskellige temperaturer, ville de relative positioner af disse kurver V vs P ændre sig i den kartesiske akse. Ændringen ville være endnu mere tydelig, hvis den blev tegnet på en tredimensionel akse, med konstant T på Z-aksen.
indeks
- 1 History of Boyle's law
- 1.1 Baggrund
- 1.2 Eksperiment med kviksølv
- 1.3 Edme Mariotte
- 1.4 Styrkelse af loven
- 2 Hvad består denne lov af??
- 3 Matematisk udtryk
- 4 Hvad er det for? Hvilke problemer løser Boyles lov??
- 4.1 Dampmaskiner
- 4.2 Drikkevarer
- 4.3 Åndedrætssystem
- 5 Eksempler (eksperimenter)
- 5.1 Eksperiment 1
- 5.2 Eksperiment 2
- 6 referencer
History of Boyle's law
baggrund
Siden forskeren Galileo Galilei gav udtryk for sin tro på forekomsten af tomhed (1638), begyndte forskerne at studere luftens og delvist hulrums egenskaber.
Den engelsk-irske kemiker Robert Boyle begyndte at studere luftegenskaber i 1638 efter at have lært, at Otto von Guericke, en tysk ingeniør og fysiker, havde bygget en luftpumpe.
Eksperiment med kviksølv
For at udføre sine studier af lufttryk brugte Boyle et glasrør i form af "J", hvis konstruktion blev tilskrevet Robert Hooke, en assistent af Boyle. Enden af den korte arm blev forseglet, mens enden af rørets lange arm var åben for at placere kviksølv.
Fra begyndelsen ønskede Boyle at studere luftens elasticitet, kvalitativt og kvantitativt. Ved at hælde kviksølv gennem den åbne ende af det "J" formede rør udledes Boyle, at luften i rørets korte arm kontraheret under kviksølvtryk.
resultater
Jo større mængden kviksølv er tilsat til røret, desto større er trykket på luften, og jo lavere er dets volumen. Boyle opnåede en negativ eksponentiel type graf for luftvolumen som en funktion af tryk.
Mens du, hvis du plotter luftens volumen mod det omvendte tryk, har du en lige linje med positiv hældning.
I 1662 udgav Boyle den første fysiske lov, der blev givet i form af en ligning, som angav den funktionelle afhængighed af to variabler. I dette tilfælde er trykket og lydstyrken.
Boyle påpegede, at der var et omvendt forhold mellem trykket udøvet på en gas og volumenet besat af den pågældende gas, hvilket forhold er relativt sandt for virkelige gasser. De fleste gasser opfører sig som ideelle gasser ved moderate tryk og temperaturer.
Med højere tryk og lavere temperaturer blev afvigelser fra idealernes virkelige gasser mere synlige.
Edme Mariotte
Den franske fysiker Edme Mariotte (1620-1684) opdagede uafhængigt den samme lov i 1679. Men det var værd at vise, at lydstyrken varierer med temperaturen. Derfor hedder det Mariotte's Law eller Boyle's og Mariotte's Law.
Styrkelse af loven
Daniel Bernoulli (1737) styrket Boyle's lov ved at påpege, at gastrykket er produceret af gaspartiklernes indvirkning på væggene i beholderen, der indeholder den..
I 1845 offentliggjorde John Waterston en videnskabelig artikel, hvori han fokuserer på de vigtigste principper for kinetisk teori om gasser.
Senere konsoliderede Rudolf Clausius, James Maxwell og Ludqwig Boltzmann kinetisk teori om gasser, der relaterer trykket udøvet af en gas med hastigheden af gasens partikler i bevægelse.
Jo mindre volumen beholderen indeholder en gas, desto større er frekvensen af virkningerne af partiklerne, der danner den mod beholderens vægge. og derfor er jo større trykket udøves af gassen.
Hvad består denne lov af??
De eksperimenter, der udføres af Boyle, påpeger, at der er et omvendt forhold mellem volumenet optaget af en gas og det tryk der udøves på det. Imidlertid er ovennævnte forhold ikke fuldstændigt lineært, som angivet ved en graf af volumenvariation ifølge det tryk, der tilskrives Boyle.
I Boyle's lov påpeges det, at volumenet optaget af en gas er omvendt proportional med trykket. Det er også angivet, at produktet af trykket af en gas ved dets volumen er konstant.
Matematisk udtryk
For at komme til matematisk udtryk for Boyle-Mariotte loven, starter vi fra:
V α 1 / P
Hvor det indikerer, at volumenet optaget af en gas er omvendt proportional med dets tryk. Der er dog en konstant der dikterer, hvordan omvendt proportional dette forhold er.
V = k / P
Hvor k er proportionalitetskonstanten. Clearing k du har:
VP = k
Produktet af trykket af en gas ved dets volumen er konstant. derefter:
V1P1 = k og v2P2 = k
Og herfra kan det udledes, at:
V1P1 = V2P2
Sidstnævnte er det endelige udtryk eller ligning for Boyle's lov.
Hvad er det for? Hvilke problemer løser Boyles lov??
Dampmaskiner

Boyle-Mariotte-loven gælder for drift af dampmotorer. Det er en ekstern forbrændingsmotor, der bruger omdannelsen af termisk energi fra en mængde vand til mekanisk energi.
Vandet opvarmes i en hermetisk forseglet kedel, og den producerede damp udøver et tryk i henhold til Boyle-Mariote-loven, der frembringer en volumenudvidelse af en cylinder ved at skubbe et stempel.
Stempelets lineære bevægelse omdannes til en rotationsbevægelse ved anvendelse af et system af vev og vev, som kan køre hjulene i et lokomotiv eller rotoren til en elektrisk generator.
I øjeblikket er den alternative dampmotor en lille brugt motor, da den er blevet forskudt af elmotoren og forbrændingsmotoren i transportkøretøjer.
Sipping drinks
Handlingen med at suge en sodavand eller saft fra en flaske gennem et plastrør er relateret til Boyle-Mariotte-loven. Når luften suges fra røret ved hjælp af munden, er der et fald i trykket inde i røret.
Dette trykfald letter væskens opadgående bevægelse i røret, hvilket tillader indtagelse. Det samme princip virker i udvindingen af blod ved hjælp af en sprøjte.
Åndedrætssystem
Boyle-Mariotte-loven er tæt knyttet til funktionen af åndedrætssystemet. Under inspirationsfasen forekommer sammentrækning af membranen og andre muskler; for eksempel de eksterne intercostaler, der frembringer en udvidelse af ribbeholderen.
Dette medfører et fald i intrapleuralt tryk, hvilket forårsager en lungekspansion, der frembringer en stigning i lungevolumen. Derfor falder det intrapulmonale tryk i overensstemmelse med det, der er angivet i Boyle-Mariotte-loven.
Når det intrapulmonale tryk er subatmosfærisk, strømmer atmosfærisk luft ind i lungerne, hvilket resulterer i øget tryk i lungerne; lig med dets tryk på atmosfærisk tryk og afsluttende fase af inspiration.
Derefter slapper de inspirerende muskler af og de ekspiratoriske muskler samler sig. Derudover opstår lungelastisk tilbagetrækning, et fænomen, der frembringer et fald i lungevolumen med en følgelig stigning i intrapulmonalt tryk, hvilket kan forklares ved Boyle-Mariotte-loven..
Ved at øge intrapulmonalt tryk og bliver større end atmosfærisk tryk, strømmer luften fra lungerne ind i atmosfæren. Dette sker, indtil trykket er udlignet, hvilket slutter udløbsfasen.
Eksempler (eksperimenter)
Eksperiment 1
En lille ballon er anbragt tæt lukket, der knytter en knude i munden, inden i en sprøjte, hvor stemplet er blevet fjernet, på ca. 20 ml. Sprøjten på sprøjten er placeret mod sprøjtens midterdel, nålen fjernes, og luftindgangen er blokeret.
observation
Ved langsomt at trække stempelet af injektoren, bemærkes det, at ballonen er oppustet.
forklaring
Der udøves to tryk på ballonens væg: et tryk på dets indvendige flade, et produkt af luften indeholdt i ballonen og et andet tryk på ballonens yderside, der udøves af luften indeholdt i sprøjten.
Når du trækker stempelet på injektoren, oprettes der et halvt vakuum inde i det. Derfor falder lufttrykket på ydersiden af pumpevæggen, hvilket gør trykket, der udøves inde i pumpen, relativt større..
Dette nettryk vil ifølge Boyle-Mariote-loven frembringe en udsparing af ballonvæggen og en stigning i ballonens volumen.
Eksperiment 2
Skær en plastikflaske, cirka halvt, så sørg for, at klippet er så vandret som muligt. I flasken er der placeret en veljusteret ballon, samtidig med at en vis mængde vand anbringes i en dyb skål.
observation
Ved at placere bunden af flasken med ballonen på skålens vand, er ballonen moderat oppustet.
forklaring
Vandet fortrænger en vis mængde luft, hvilket øger trykket af luften på flaskevæggen og det indre af ballonen. Dette forårsager ifølge Boyle-Mariotte-loven en stigning i verdensmængden, som er visualiseret af verdens inflation.
referencer
- Wikipedia. (2019). Boyle's lov. Hentet fra: en.wikipedia.org
- Editors of Encyclopaedia Britannica. (27. juli 2018). Boyle's lov. Encyclopædia Britannica. Hentet fra: britannica.com
- Helmenstine, Todd. (5. december 2018). Formlen for Boyles lov. Hentet fra: thoughtco.com
- Unge indiske film. (15. maj 2018). Boyle's Law: Science Experiment for Kids. Hentet fra: yifindia.com
- Cecilia Bembibre (22. maj 2011). Varmluftsballon Definition ABC. Hentet fra: definicionabc.com
- Ganong, W, F. (2003). Medicinsk Fysiologi (19. udgave). Editorial the Modern Manual.


