Sølvoxid (Ag2O) struktur, egenskaber, nomenklatur og anvendelser
den sølvoxid er en uorganisk forbindelse, hvis kemiske formel er Ag2O. Den kraft, der forener dets atomer, er af en fuldstændig ionisk natur; Derfor består den af et ionisk fast stof, hvor der er et forhold på to Ag kationer+ interagerer elektrostatisk med en anion O2-.
Oxidanionet, O2-, det skyldes samspillet mellem sølvatomer i overfladen og miljøets ilt; på en meget lignende måde som jern og mange andre metaller. En sølvbit eller smykker i stedet for rødme og smuldrer i rust, bliver sort, karakteristisk for sølvoxid.

For eksempel i billedet ovenfor kan du se en rusten sølvkop. Bemærk dens mørkede overflade, selvom den stadig bevarer nogle prydende glans; Derfor kan selv rustne sølvgenstande betragtes som attraktive nok til dekorative anvendelser.
Egenskaberne af sølvoxid er således, at de ikke ved første øjekast ødelægger den oprindelige metalliske overflade. Den dannes ved stuetemperatur ved simpel kontakt med iltet i luften; og endnu mere interessant, kan det nedbrydes ved høje temperaturer (over 200 ° C).
Det betyder, at hvis billedets glas blev holdt, og varmen fra en intens flamme blev påført, ville den genvinde sin sølvfarvede glans. Derfor er dens dannelse en termodynamisk reversibel proces.
Sølvoxid har også andre egenskaber og ud over sin enkle Ag-formel2Eller det omfatter komplekse strukturelle organisationer og et rigt udvalg af faste stoffer. Imidlertid er Ag2Eller er det måske ved siden af Ag2O3, den mest repræsentative for sølvoxiderne.
indeks
- 1 Sølvoxidstruktur
- 1.1 Ændringer med antallet af valencia
- 2 Fysiske og kemiske egenskaber
- 2,1 Molekylvægt
- 2.2 Udseende
- 2.3 Tæthed
- 2.4 Smeltepunkt
- 2,5 kps
- 2.6 Opløselighed
- 2,7 kovalent karakter
- 2,8 nedbrydning
- 3 nomenklaturen
- 3.1 Valencias I og III
- 3.2 Systematisk nomenklatur for komplekse sølvoxider
- 4 anvendelser
- 5 referencer
Struktur af sølvoxid
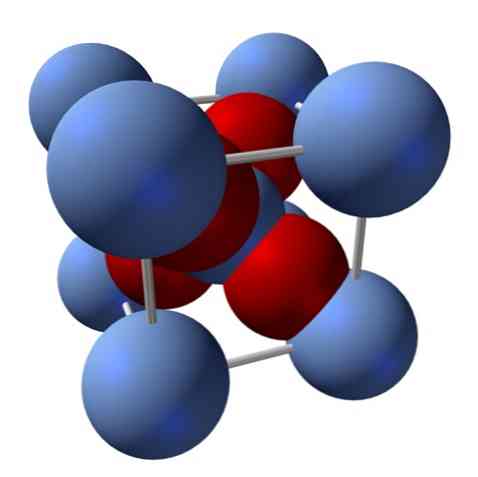
Hvordan er dens struktur? Som nævnt i begyndelsen: Det er et ionisk faststof. Af denne grund kan der ikke være kovalente bindinger Ag-O eller Ag = O i dets struktur; da, hvis der var, ville egenskaberne af dette oxid ændre sig drastisk. Det er så Agioner+ og o2- i et 2: 1 forhold og oplever en elektrostatisk attraktion.
Sølvoxidets struktur bestemmes som følge af den måde, hvorpå de ioniske kræfter disponerer i rummet Agionerne+ og o2-.
I det øverste billede har du for eksempel en enhedscelle til et kubisk krystallinsk system: Ag kationerne+ er de sølvblå kugler og O.2- de rødlige sfærer.
Hvis du tæller antallet af kugler, vil du opdage, at der ved første øjekast er ni af sølvblå og fire røde farver. Imidlertid tages kun fragmenterne af kuglerne inde i terningen i betragtning; at tælle disse, idet de er fraktioner af de samlede sfærer, skal forholdet 2: 1 for Ag være opfyldt2O.
Gentagelse af AgO-tetrahedronens strukturelle enhed4 omgivet af fire andre Ag+, alt det sorte faststof er bygget (fjernelse af hullerne eller uregelmæssighederne, som disse krystalordninger kan have).
Ændringer med antallet af valencia
Fokuserer nu ikke på AgO tetraederen4 men i AgOAg linje (se toppunkterne i den øvre hub), vil have den faste sølvoxid består, fra et andet perspektiv, flerlags ion anbragt lineært (selvom tilbøjelige). Alt dette som et resultat af den "molekylære" geometri omkring Ag+.
Ovennævnte er blevet bekræftet af flere undersøgelser af dens ioniske struktur.
Sølv arbejder overvejende med valens +1, da når man mister en elektron, er den resulterende elektroniske konfiguration [Kr] 4d10, som er meget stabil. Andre valenser, såsom Ag2+ og Ag3+ de er mindre stabile, da de mister elektroner fra orbitaler næsten fuldstændigt fyldt.
Agionen3+, Det er dog relativt mindre ustabil i forhold til Ag2+. Faktisk kan den eksistere sammen med Ag+ Kemisk berigelse af strukturen.
Den elektroniske konfiguration er [Kr] 4d8, med opparerede elektroner på en sådan måde, at den giver en vis stabilitet.
I modsætning til lineære geometrier omkring Agioner+, Det er blevet fundet, at Agionernes3+ Det er firkantet fladt. Derfor et sølvoxid med Ag ioner3+ ville bestå af lag sammensat af AgO kvadrater4 (ikke tetrahedra) elektrostatisk koblet af AgOAg linjer; Sådan er tilfældet med Ag4O4 eller Ag2O ∙ Ag2O3 med monoklinisk struktur.
Fysiske og kemiske egenskaber

Hvis overfladen af sølvet cup skrabet hovedbilledet, et fast stof, som ikke kun er sort, men også har opnås brune eller brune (øverst) nuancer. Nogle af dens fysiske og kemiske egenskaber rapporteret af øjeblikket er følgende:
Molekylvægt
231.735 g / mol
udseende
Massiv sort brun i pulverform (bemærk at det mangler et krystallinsk udseende på trods af at det er et ionisk fast stof). Det er lugtfri og blandet med vand giver det en metallisk smag
tæthed
7,14 g / ml.
Smeltepunkt
277-300 ° C. Det smelter sikkert i fast sølv; det vil sige, det bryder sandsynligvis ned før dannelse af flydende oxid.
KPS
1,52 ∙ 10-8 i vand ved 20 ° C. Det er derfor en forbindelse, der næppe er opløselig i vand.
opløselighed
Hvis du ser omhyggeligt på billedet af dets struktur, vil du opdage, at sfærerne af Ag2+ og o2- De er ikke uenige næsten i størrelse. Som et resultat kan kun små molekyler trænge ind i det krystallinske gitters indre, hvilket gør det uopløseligt i næsten alle opløsningsmidler; bortset fra dem, hvor det reagerer, såsom baser og syrer.
Kovalent karakter
Selv om det gentagne gange er blevet sagt, at sølvoxid er en ionforbindelse, modsætter visse egenskaber, såsom dets lave smeltepunkt, denne erklæring.
Overvejelsen af den kovalente karakter bryder bestemt ikke ned, hvad der forklares for dets struktur, det ville være nok at tilføje det til strukturen af Ag2Eller en model af kugler og søjler for at indikere kovalente bindinger.
Også tetrahedra og firkantede fly AgO4, såvel som AgOAg linjerne, ville de være bundet af kovalente (eller kovalente ioniske) bindinger.
Med dette i betragtning er Ag2Eller det ville faktisk være en polymer. Det anbefales dog at betragte det som et ionisk faststof med kovalent karakter (hvis art af forbindelsen stadig er en udfordring i dag).
nedbrydning
I starten blev det nævnt, at dets dannelse er termodynamisk reversibel, så det absorberer varme for at vende tilbage til dets metalliske tilstand. Alt dette kan udtrykkes af to kemiske ligninger for sådanne reaktioner:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2AG2O (s) + Q => 4Ag (s) + O2(G)
Hvor Q repræsenterer varmen i ligningen. Dette forklarer hvorfor branden, der brænder overfladen af den rustede sølvkopper, returnerer sin sølvfarvede glans.
Derfor er det svært at antage, at der er Ag2O (l) da det ville nedbrydes øjeblikkeligt ved varme; medmindre trykket er for højt til opnåelse af den brune sorte væske.
nomenklatur
Når muligheden for Agioner blev introduceret2+ og Ag3+ ud over den fælles og dominerende ag+, Begrebet "sølvoxid" begynder at virke utilstrækkeligt til at henvise til Ag2O.
Dette skyldes, at Agion+ er mere rigelig end de andre, så Ag er taget2Eller som det eneste oxid; hvilket slet ikke er korrekt.
Hvis du overvejer Ag2+ som praktisk taget ikke-eksisterende med sin ustabilitet, vil kun ionerne med valenser +1 og +3 være til stede; det vil sige Ag (I) og Ag (III).
Valencias I og III
At være Ag (I) den mindste valens, det er navngivet ved at tilføje suffixet -os til dets navn Argentum. Så Ag2Eller det er: argentoso oxid eller, ifølge den systematiske nomenklatur, diplomatmonoxid.
Hvis Ag (III) fuldstændig ignoreres, skal dens traditionelle nomenklatur være: sølvoxid i stedet for argentinoxid.
På den anden side er Ag (III) den større valens tilføjet suffiksen -ico til dens navn. Så Ag2O3 er: sølvoxid (2 Ag ioner)3+ med tre o2-). Også dets navn i henhold til den systematiske nomenklatur ville være: diplatatrioxid.
Hvis strukturen af Ag observeres2O3, det kan antages at det er produktet af oxidation af ozon, OR3, i stedet for ilt. Derfor skal dens kovalente karakter være større, da den er en kovalent forbindelse med Ag-O-O-O-Ag eller Ag-O-bindinger.3-Ag.
Systematisk nomenklatur for komplekse sølvoxider
AgO, også skrevet som Ag4O4 eller Ag2O ∙ Ag2O3, Det er et sølvoxid (I, III), da det har begge værdier +1 og +3. Dets navn i henhold til den systematiske nomenklatur ville være: tetraplate tetraoxid.
Denne nomenklatur er til stor hjælp, når det gælder andre støkiometrisk mere komplekse sølvoxider. Antag for eksempel de to faste stoffer 2Ag2O ∙ Ag2O3 og Ag2O ∙ 3Ag2O3.
At skrive den første på en mere passende måde ville være: Ag6O5 (tælling og tilsætning af atomer af Ag og O). Hans navn ville så være hexaplatpentoxid. Bemærk at dette oxid har en sølv sammensætning mindre rig end Ag2O (6: 5 < 2:1).
Mens du skriver det andet faste andet, ville det være: Ag8O10. Dets navn ville være octaplat-decaoxid (med et forhold på 8:10 eller 4: 5). Dette hypotetiske sølvoxid ville være "meget oxideret".
applikationer
Undersøgelser på jagt efter nye og sofistikerede anvendelser til sølvoxid udføres stadig i dag. Nogle af dens anvendelser er anført nedenfor:
-Det opløses i ammoniak, ammoniumnitrat og vand til dannelse af Tollens-reagenset. Dette reagens er et nyttigt redskab i kvalitative analyser inden for organiske kemi laboratorier. Det gør det muligt at bestemme tilstedeværelsen af aldehyder i en prøve, idet det positive svar er dannelsen af et "sølvspejl" i reagensrøret.
-Sammen med metallisk zink danner det de primære batterier af zinkoxid af sølv. Dette er måske en af de mest almindelige og hjemlige anvendelser.
-Det tjener som en gasrensning, der absorberer for eksempel CO2. Når den opvarmes, frigør den de fangne gasser og kan genanvendes flere gange.
-På grund af sølvs antimikrobielle egenskaber er dets oxid nyttigt i studier af bioanalyse og jordrensning.
-Det er et mildt oxidationsmiddel, der er i stand til at oxidere aldehyder til carboxylsyrer. Det anvendes også i Hofmann-reaktionen (tertiære aminer) og deltager i andre organiske reaktioner, enten som reagens eller katalysator.
referencer
- Bergstresser M. (2018). Sølvoxid: Formel, nedbrydning og dannelse. Undersøgelse. Hentet fra: study.com
- Forfattere og redaktører af bindene III / 17E-17F-41C. (N.D.). Sølvoxider (Ag (x) O (y)) krystalstruktur, gitterparametre. (Numeriske Data og Funktionelle Forhold i Videnskab og Teknologi), vol. 41C. Springer, Berlin, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Potentielle virkninger af biofelt-energibehandling på de fysiske og termiske egenskaber ved sølvoxidpulver. International Journal of Biomedical Science and Engineering. Bind 3, nr. 5, s. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Nedbrydning af sølvoxid. University of Oregon Hentet fra: chemdemos.uoregon.edu
- Flint, Deyanda. (24. april 2014). Anvendelse af sølvoxidbatterier. Sciencing. Hentet fra: sciencing.com
- Salman Montasir E. (2016). Undersøgelse af nogle optiske egenskaber ved sølvoxid (Ag2o) ved anvendelse af UVVisible spektrofotometer. [PDF]. Hentet fra: iosrjournals.org
- Bard Allen J. (1985). Standardpotentialer i vandig opløsning. Marcel Dekker. Hentet fra: books.google.co.ve


