Kaliumjodoat Egenskaber, struktur, anvendelser og risici
den kaliumiodat eller kaliumjodat er en uorganisk forbindelse af iod, specifikt et salt, hvis kemiske formel er KIO3. Jodelementet i gruppen af halogener (F, Cl, Br, I, As) har i dette salt et oxidationsnummer på +5; På grund af dette er det et stærkt oxidationsmiddel. KIO3 dissocieres i vandigt medium for at skabe K-ionerne+ og IO3-.
Den syntetiseres ved at reagere kaliumhydroxid med iodsyre: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Det kan også syntetiseres ved at reagere molekylært iod med kaliumhydroxid: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

indeks
- 1 Fysiske og kemiske egenskaber
- 1.1 Oxiderende middel
- 2 Kemisk struktur
- 3 Anvendelser og anvendelser af kaliumjodat
- 3.1 Terapeutisk anvendelse
- 3.2 Anvendelse i branchen
- 3.3 Analytisk anvendelse
- 3.4 Anvendelse i laserteknologi
- 4 Sundhedsrisici ved kaliumiodat
- 5 referencer
Fysiske og kemiske egenskaber
Det er et lugtfri hvidt fast stof med fine krystaller og en krystallinsk struktur af monoklinisk type. Den har en densitet på 3,98 g / ml, en molekylvægt på 214 g / mol og har absorptionsbånd i det infrarøde (IR) spektrum.
Den har et smeltepunkt: 833 ºK (560 ºC), i overensstemmelse med de stærke ioniske vekselvirkninger mellem K ionerne+ og IO3-. Ved højere temperaturer gennemgår den en termisk dekomponeringsreaktion, der frigiver molekylært oxygen og kaliumiodid:
2KIO3(s) => 2KI (s) + 3O2(G)
Det har opløseligheder i vand i området fra 4,74g / 100 ml til 0 ° C, til 32,3 g / 100 ml til 100 ° C, generatorer farveløse vandige opløsninger. Derudover er det uopløseligt i alkohol og salpetersyre, men er opløseligt i fortyndet svovlsyre.
Dens affinitet for vand er ikke mærkbar, hvilket forklarer hvorfor det ikke er hygroskopisk og eksisterer ikke i form af hydreret salte (KIO)3· H2O).
Oxiderende middel
Kaliumjodat, som angivet ved dets kemiske formel, har tre oxygenatomer. Dette er et stærkt electronegative element og på grund af denne egenskab "afslører" en elektronisk mangel i skyen omkring joden.
Denne mangel eller input, som i hvert enkelt kan beregnes som antallet af oxidation af iod (± 1, 2, 3, 5, 7), er 5 i tilfælde af dette salt.
Hvad betyder dette? At før en art, der er i stand til at give sine elektroner, vil jod acceptere dem i deres ioniske form (IO3-) for at blive molekylært iod og have et oxidationsnummer lig med 0.
Efter denne forklaring kan det bestemmes, at kaliumiodat er en oxiderende forbindelse, der reagerer kraftigt med mange reduktionsmidler i redoxreaktioner; af alle disse er man kendt som jodklokken.
Jodklokken består af en redox-proces med langsomme og hurtige trin, hvor de hurtige trin er markeret med en KIO-løsning3 i svovlsyre, hvortil der tilsættes stivelse. Dernæst stivelsen - en gang produceret og forankret mellem dens strukturart I3-- vil ændre opløsningen fra farveløs til mørkblå.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6 H+ → 3 I2 + 3 H2O
jeg2 + HSO3- + H2O → 2 I- + HSO4- + 2 H+ (mørk blå på grund af stivelseseffekt)
Kemisk struktur
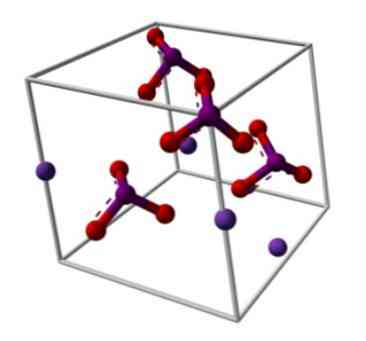
Den kemiske struktur af kaliumiodat er illustreret i det øvre billede. IO-anionen3- er repræsenteret af "stativet" af røde og lilla kugler, mens K ionerne+ de er repræsenteret af de lilla kugler.
Men hvad betyder disse stativ? De korrekte geometriske former af disse anioner er faktisk trigonale pyramider, hvori oxygenatomerne danner trekantede base, og den udelt elektronpar jod peger opad, besætter plads og tvinge fold ned IO linket og de to links I = O.
Denne molekylære geometri svarer til en sp hybridisering3 af det centrale iodatom; et andet perspektiv antyder imidlertid, at et af oxygenatomerne danner bindinger med jodens "d" orbitaler, der faktisk er en sp hybridisering3d2 (jodet kan have sine "d" orbitaler udvide sin valence shell).
Krystallerne af dette salt kan gennemgå overgange af strukturfase (andre arrangementer end monokliniske) som følge af de forskellige fysiske betingelser, der udsætter dem.
Anvendelser og anvendelser af kaliumjodat
Terapeutisk anvendelse
Kaliumjodat bruges normalt til at forhindre akkumulering af radioaktivitet i skjoldbruskkirtlen i form af 131Jeg, når denne isotop anvendes til bestemmelse af iodoptagelse af skjoldbruskkirtlen som en bestanddel af funktionen af skjoldbruskkirtlen.
Ligeledes anvendes kaliumiodat som et topisk antiseptisk middel (0,5%) i slimhindeinfektioner.
Brug i branchen
Det tilsættes til foderet fra husdyrene som et jodtilskud. Derfor anvendes kaliumjodat i branchen til at forbedre kvaliteten af melet.
Analytisk anvendelse
I analytisk kemi, takket være stabiliteten, anvendes den som en primær standard i standardiseringen af natriumthiosulfat standardopløsninger (Na2S2O3) for at bestemme koncentrationerne af iod i prøverne.
Dette betyder, at mængden af jod kan kendes ved hjælp af volumetriske teknikker (titreringer). I denne reaktion oxiderer kaliumiodat hurtigt jodidioner I-, ved den følgende kemiske ligning:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jod, jeg2, er titlen med opløsningen af Na2S2O3 for dets standardisering.
Anvendes i laserteknologi
Undersøgelser har vist og bekræftet interessant piezoelektriske egenskaber, pyroelektriske, elektrooptisk, ferroelektriske og ikke-lineær optik krystaller KIO3. Dette resulterer i stort potentiale på det elektroniske område og i teknologien til lasere til materialer fremstillet med denne forbindelse.
Sundhedsrisici ved kaliumiodat
I høje doser kan det forårsage irritation i mundslimhinden, huden, øjnene og luftveje.
Eksperimenter toksiciteten af kaliumiodid i dyr har tilladt at konstatere, at i fastende hunde i doser på fra 0,2 til 0,25 g / kg legemsvægt, leveres oralt, det forårsager opkastning forbindelse.
Hvis disse opkast undgås, forårsager det en forværring af situationen i dyrene, da det fremkalder anoreksi og prostration inden døden. Hans obduktioner tilladt at observere nekrotiske læsioner i leveren, nyrerne og tarmslimhinden.
På grund af dets oxiderende effekt udgør den en brandrisiko, når den kommer i kontakt med brændbare materialer.
referencer
- Day, R., & Underwood, A. Kvantitativ Analytisk Kemi (femte udgave). PEARSON Prentice Hall, p-364.
- Muth, D. (2008). Lasere. [Figur]. Hentet fra: flickr.com
- ChemicalBook. (2017). Kaliumjodat. Hentet den 25. marts 2018 fra ChemicalBook: chemicalbook.com
- Pubchem. (2018). Kaliumjodat. Hentet den 25. marts 2018, fra PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Kaliumjodat. Hentet den 25. marts 2018 fra Merck:
- merckmillipore.com
- Wikipedia. (2017). Kaliumjodat. Hentet den 25. marts 2018, fra Wikipedia: en.wikipedia.org
- M M Abdel Kader et al. (2013). Charge transport mekanisme og lav temperatur fase overgange i KIO3. J. Phys.: Conf. Ser. 423 012036


