Proteinase K egenskaber, enzymatisk aktivitet og applikationer
den proteinase K er et enzym, der tilhører gruppen af serinproteaser, det vil sige at den i sit aktive katalytiske center har en aminosyre serin og har funktionen til at bryde peptidbindingerne ved hydrolyse. Til gengæld tilhører dette enzym familien af proteiner subtilisiner (peptidase S8).
Proteinase K har en molekylvægt (MW) på 28.900 dalton og blev isoleret for første gang i 1974 fra ekstrakter af svampen Engyodontium album, tidligere kendt ved navnet på Tritirachium-album Limber.
Det præsenterer en høj proteolytisk kapacitet, som demonstreres for at kunne nedbryde den keratin, der er til stede i håret. Ordet keratin på engelsk er skrevet "keratin", derfor er det blevet kaldt "proteinase K".
På grund af dets høje kapacitet til at spalte native proteiner er dette enzym nyttigt i forskellige molekylærbiologi teknikker. Det anvendes hovedsageligt til at isolere og forberede nukleinsyrer med høj molekylvægt (MW).
Proteinase K virker ved at frigive det nukleare DNA, samtidig med at proteinerne ødelægges og inaktiverer RNaser og DNaser, det vil sige eliminerer nucleaserne i DNA- og RNA-præparaterne..
På den anden side er det blevet set, at proteinase K kan hydrolyse nogle denaturerede native proteiner, hvilket har skabt forskernes interesse for dets anvendelse i studiet af prionproteiner (PrPC).
Men på trods af sin høje styrke findes proteolytiske proteiner, som er resistente over for virkningen af proteinase K. Blandt dem, nogle unormale proteiner kaldet prioner (PrPSc) i forbindelse med TSE er.
indeks
- 1 Karakteristik af proteinase K
- 2 Enzymatisk aktivitet
- 3 applikationer
- 4 Fordele ved proteinase K
- 5 Proteinase-resistente proteiner K
- 6 referencer
Karakteristik af proteinase K
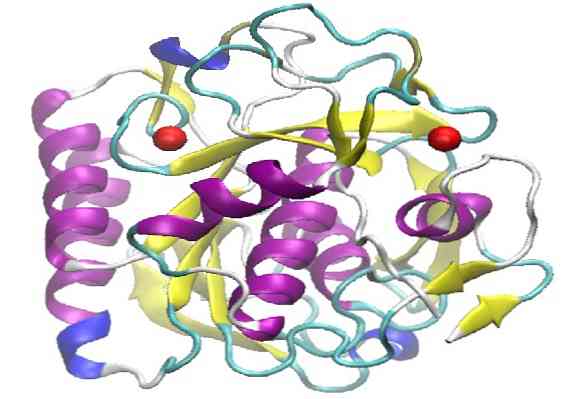
Proteinase K har en tertiær struktur dannet af tre lag, hvor et β-ark med syv kæder er spredt mellem to lag af spiraler. Fordi det tilhører familien af S8-peptidaser, er det karakteriseret ved at have en katalytisk triad i sit aktive sted, hvis sekventielle rækkefølge er (Asp, His og Ser), som differentierer dem fra andre familier af peptidaser..
Dette enzym fra gruppen af serinproteaser karakteriseres ved hydrolyse af peptidbindinger tæt på carboxylgruppen af de alifatiske og aromatiske aminosyrer.
Desuden er den i stand til at virke i nærvær af visse ætsende, såsom natriumdodecylsulfat (SDS), Tris-HCL og EDTA, som bruges til at hjælpe denatureringen af proteiner, at de mister deres native struktur stoffer.
Dette er et indledende trin i fremstillingen af proteiner til elektroforese-teknikken. PH-området, hvor proteinase K virker, er ret bred (2,0 til 12,0), med en optimal pH mellem 7,5 og 12,0, og dets isoelektriske punkt er 8,9. Som det kan ses, er det aktivt mod en meget bred pH-værdi.
En anden egenskab, der skiller sig ud i proteinase K, er dens stabilitet i nærværelse af høje temperaturer (50-60 ° C).
Enzymatisk aktivitet
Proteinase K kræver tilstedeværelse af calciumion, selv om dette ikke påvirker dets aktivitet, hvis det er vigtigt at opretholde stabiliteten.
For at protease K skal udføre den fuldstændige fordøjelse af substratet, er en omtrentlig kontakttid på mellem 5 minutter og 2 timer nødvendig.
I denne sammenhæng sammenlignede Daza et al. Sammenlignet med renheden af DNA'et opnået ved adskillige gange med eksponering for proteinase K og konkluderede, at en langvarig inkubation (op til 24 timer) signifikant forbedrer kvaliteten af DNA.
Nu, i forhold til den koncentration, der anvendes af proteinase K-enzymet i de forskellige protokoller, kan det siges, at det er meget varieret.
Det kan anvendes fra meget lave koncentrationer (5 μg / ml) til koncentrationer på 500 μg / ml. Men de hyppigste arbejdskoncentrationer ligger på mellem 50-100 μg / ml, især til proteinfordøjelse og nuklease inaktivering. Selvom der kræves en koncentration på 2 mg / ml til vævsbehandling.
applikationer
Dens applikationer er meget brede og kan opsummeres i følgende:
-Det anvendes i fordøjelsen af proteiner og DNA-ekstraktionsmetoder som er flere: udsaltning, PK-SDS, cetyltrimethylammoniumbromid ammoniumbromid (CTAB), og kaliumacetat modificeret ekstraktion med natriumiodid.
-Inaktivering af nucleaser (RNaser og DNaser).
-I hybridiseringsteknikken in situ (HIS), for at hjælpe med at frigive nukleinsyren, udover at eliminere uønskede proteiner.
-Protein modifikation.
-På forskerniveau i forskellige undersøgelser.
Fordele ved proteinase K
Flere komparative undersøgelser er blevet udført blandt DNA-ekstraktionsteknikker ved anvendelse af Proteinase K, med andre, der ikke bruger det, og alle konkluderer, at der er større fordele ved anvendelse af enzymet. Blandt fordelene kan følgende nævnes:
-DNA med høj molekylvægt af høj kvalitet og renhed opnås.
-Det ekstraherede DNA er stabilt i op til 3 måneder.
Det ekstraherede DNA kan anvendes i følgende teknikker: Southern blot, polymerasekædereaktion (PCR), elektroforese, blandt andre.
Proteiner resistente over for proteinase K
Forskellige undersøgelser har konkluderet, at prioner (unormale PrPSc-toksiske proteiner) differentieres fra PrPC-proteiner (native), fordi de er resistente over for proteinase K's virkning, mens PrPC er følsomme for deres virkning.
Andre forfattere har beskrevet, at der i strukturen af PrPSc er følsomme dele og andre resistente overfor proteinase K. Imidlertid er begge dele lige giftige og infektive..
På den anden side isolerede Bastian og samarbejdspartnere i 1987 4 proteiner på 28, 30, 66 og 76 kda fra en art af Spiroplasma mirum. Alle var resistente over for virkningen af proteinase K og havde også en krydsreaktion med nogle prioner.
Det er kendt, at denne art kan forårsage grå stær og betydelige neurologiske skader og på grund af videnskabelige resultater Bastian, blandt andet forskning, har forsøgt at linke til denne mikroorganisme med overførbare spongiforme encephalopatier.
Imidlertid er etiologien af denne degenerative neurologiske patologi stadig tilskrives prioner i dag.
I denne forbindelse identificerede Butler og samarbejdspartnere i 1991 og karakteriserede en klasse af 40 Kda proteinase resistent protein K fra to stammer af Mycoplasma hyorhinis. Dette patogen påvirker svinene, inficerer deres væv, men i dette tilfælde var der ingen krydsreaktion med de testede prioner.
Mere forskning er nødvendig for at belyse mange ukendte om det.
referencer
- Bastian F, Jennings R og Gardner W. 1987. Antiserum til scrapieassocieret fibrilprotein krydsreagerer med Spiroplasma mirum fibrilproteiner. J. Clin. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Evaluering af en DNA-ekstraktions- og oprensningsmetode fra muskelvæv fastgjort i formaldehyd fra ukendte cadavers. Med Magazine, 2014, 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E og Mcgarrity G. Identifikation og karakterisering af proteasease K-resistente proteiner i medlemmer af klassens mollicutes. Infektion og immunitet, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et al. Sammenligning af to protokoller til ekstraktion af DNA fra Trypanosoma cruzi dyrket i aksenisk medium. Rev. Peru. Med. Udl. Folkesundhed 2014, 31 (2): 222-227. Tilgængelig på: scielo.org
- Jiménez G, Villalobos M, Jiménez E og Palma W. Bestemmelse af effektiviteten af fem DNA-ekstraktionsprotokoller fra paraffinmateriale til molekylære undersøgelser. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


