Ethylacetatstruktur, egenskaber, syntese, anvendelser og risici
den ethylacetat eller ethylethanoat (IUPAC-navn) er en organisk forbindelse, hvis kemiske formel er CH3COOC2H5. Den består af en ester, hvor alkoholkomponenten stammer fra ethanol, mens dens carboxylsyrebestanddel kommer fra eddikesyre.
Det er en væske under normale betingelser for temperatur og tryk, der præsenterer en behagelig aroma til frugt. Denne ejendom går perfekt i harmoni med hvad der forventes af en ester; som faktisk er den kemiske karakter af ethylacetat. Af denne grund finder den anvendelse i fødevarer og alkoholholdige drikkevarer.
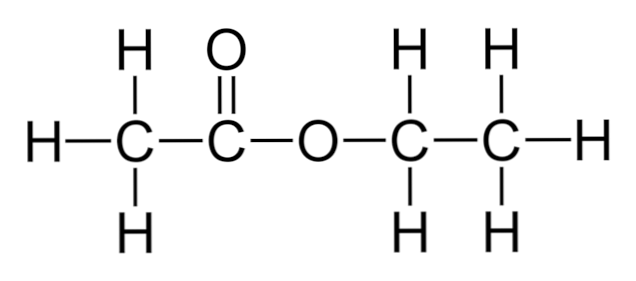
I det øvre billede er strukturskeletet af ethylacetat vist. Bemærk til venstre sin carboxylsyre komponent, og til højre alkoholkomponenten. Fra et strukturelt synspunkt kan det forventes, at denne forbindelse opfører sig som en hybrid mellem eddike og alkohol; Det udviser dog egenskaber.
Det er her, hvor sådanne hybrider kaldes estere skiller sig ud som værende forskellige. Ethylacetat kan ikke reagere som en syre, og det kan heller ikke dehydrere i fravær af en OH-gruppe. I stedet undergår den basisk hydrolyse i nærværelse af en stærk base, såsom natriumhydroxid, NaOH.
Denne hydrolysereaktion anvendes i undervisningslaboratorier til kemiske kinetiske forsøg; hvor reaktionen desuden er af anden rækkefølge. Når hydrolyse opstår, vender praktisk taget ethylethanoat tilbage til dets indledende komponenter: syre (deprotoneret med NaOH) og alkohol.
I dets strukturelle skelet bemærkes det, at hydrogenatomer dominerer over oxygenindholdet. Dette påvirker deres evne til at interagere med ikke-polære arter som fedtstoffer. Det anvendes også til opløsning af forbindelser som harpikser, farvestoffer og generelt organiske faste stoffer.
På trods af en behagelig aroma frembringer en langvarig eksponering for denne væske en negativ indvirkning (som næsten alle kemiske forbindelser) i kroppen.
indeks
- 1 Struktur af ethylacetat
- 1.1 Manglende hydrogendonoratomer
- 2 Fysiske og kemiske egenskaber
- 2.1 Navne
- 2,2 Molekylformel
- 2,3 Molekylvægt
- 2.4 Fysisk beskrivelse
- 2,5 farve
- 2.6 lugt
- 2,7 Smag
- 2,8 lugtgrænsen
- 2,9 kogepunkt
- 2,10 Smeltepunkt
- 2.11 Opløselighed i vand
- 2.12 Opløselighed i organiske opløsningsmidler
- 2.13 Tæthed
- 2.14 Damptæthed
- 2,15 Stabilitet
- 2.16 Damptryk
- 2,17 Viskositet
- 2.18 Forbrændingsvarme
- 2.19 Fordampningsvarme
- 2.20 Overfladespænding
- 2.21 Brekningsindeks
- 2.22 Opbevaringstemperatur
- 2,23 pKa
- 3 Sammenfatning
- 3.1 Fishers reaktion
- 3.2 Tishchenko reaktion
- 3.3 Andre metoder
- 4 anvendelser
- 4.1 Opløsningsmiddel
- 4.2 Kunstige smagsstoffer
- 4.3 Analytics
- 4.4 Organisk syntese
- 4.5 kromatografi
- 4.6 Entomologi
- 5 risici
- 6 referencer
Struktur af ethylacetat
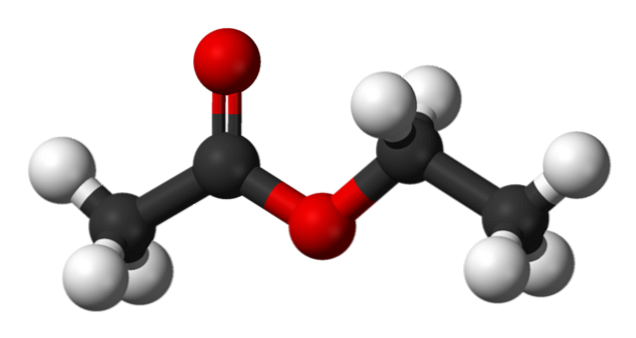
I det øvre billede er strukturen af ethylacetat vist med en model af kugler og søjler. I denne model fremhæves oxygenatomer med røde kugler; til venstre er fraktionen afledt af syren, og til højre er den fraktion afledt af alkohol (alkoxygruppe -OR).
Carbonylgruppen er værdsat af C = O-bindingen (de dobbelte stænger). Strukturen omkring denne gruppe og det tilstødende ilt er fladt, fordi der er en delokalisering af belastningen ved resonans mellem begge oxygener; faktum, der forklarer en relativt lav surhed af a-hydrogenerne (dem af -CH-gruppen3, knyttet til C = O).
Molekylet, ved at rotere to af sine bindinger, favoriserer direkte, hvordan det interagerer med andre molekyler. Tilstedeværelsen af de to oxygenatomer og asymmetrien i strukturen giver den et permanent dipolmoment; som igen er ansvarlig for deres dipole-dipol interaktioner.
For eksempel er den elektroniske tæthed større nær de to oxygenatomer, hvilket falder betydeligt i gruppen -CH3, og gradvist i OCH-gruppen2CH3.
På grund af disse interaktioner danner ethylacetatmolekylerne en væske under normale forhold, som har et betydeligt højt kogepunkt (77ºC).
Fravær af donoratomer af hydrogenbindinger
Hvis du ser tæt på strukturen, vil du bemærke manglen på et atom, der er i stand til at donere en brintbro. Oxygenatomer er imidlertid sådanne acceptorer, og ethylacetat er meget opløseligt i vand og interagerer i betydelig grad med polære forbindelser og hydrogenbindende donorer (såsom sukkerarter).
Dette giver dig også mulighed for at interagere godt med ethanol; hvorfor dets tilstedeværelse i alkoholholdige drikkevarer ikke er overraskende.
På den anden side gør sin alkoxygruppe det i stand til at interagere med visse apolære forbindelser, såsom chloroform, CH3cl.
Fysiske og kemiske egenskaber
navne
-Ethylacetat
-Ethylethanoat
-Eddikesyreester
-Acetoxietano
Molekylformel
C4H8O2 eller CH3COOC2H5
Molekylvægt
88.106 g / mol.
Fysisk beskrivelse
Klar farveløs væske.
farve
Farveløs væske.
lugt
Karakteristisk for ethere, ligner duften af ananas.
smag
Behageligt når fortyndet, tilføjer en frugtagtig smag til øl.
Lugtgrænsen
3,9 ppm. 0,0196 mg / m3 (lav lugt); 665 mg / m3 (høj lugt).
Detekterbar lugt ved 7 - 50 ppm (middel = 8 ppm).
Kogepunkt
171 ° F til 760 mmHg (77,1 ° C).
Smeltepunkt
-118,5 ºF (-83,8 ºC).
Opløselighed i vand
80 g / l.
Opløselighed i organiske opløsningsmidler
Blandbar med ethanol og ethylether. Meget opløselig i acetone og benzen. Blandbar også med chloroform, faste og flygtige olier, og også med iltede og chlorerede opløsningsmidler.
tæthed
0,9003 g / cm3.
Damptæthed
3,04 (i luftforhold: 1).
stabilitet
Den nedbrydes langsomt med fugtighed; uforenelig med flere plastik og stærke oxidationsmidler. Blandingen med vand kan være eksplosiv.
Damptryk
93,2 mmHg ved 25 ºC
viskositet
0,423 mPoise ved 25 ºC.
Forbrændingsvarme
2.238,1 kJ / mol.
Fordampningsvarme
35,60 kJ / mol ved 25 ºC.
Overfladespænding
24 dyn / cm ved 20 ºC.
Brydningsindeks
1.373 ved 20 ºC / D.
Opbevaringstemperatur
2 - 8 ºC.
pKa
16-18 ved 25 ºC.
syntese
Fisher's reaktion
Ethylacetat syntetiseres industrielt ved Fisher-reaktionen, hvor ethanol er esterificeret med eddikesyre. Reaktionen udføres ved stuetemperatur.
CH3CH2OH + CH3COOH <=> CH3COOCH2CH3 + H2O
Reaktionen accelereres ved syrekatalyse. Ligevægten bevæger sig til højre, det vil sige i retning af produktionen af ethylacetat gennem fjernelse af vand; i henhold til loven om massehandling.
Reaktion af Tishchenko
Ethylacetat fremstilles også industrielt under anvendelse af Tishchenko-reaktionen, der konjugerer to ækvivalenter acetaldehyd ved anvendelse af et alkoxid som katalysator.
2 CH3CHO => CH3COOCH2CH3
Andre metoder
-Ethylacetat syntetiseres som et coprodukt i oxidationen af butan til eddikesyre i en reaktion udført ved en temperatur på 175 ° C og 50 atm tryk. Cobalt og kromioner anvendes som katalysator.
-Ethylacetat er et coprodukt af ethanolysen af polyvinylacetat til polyvinylalkohol.
-Ethylacetat fremstilles også i industrien ved dehydrogenering af ethanol, idet reaktionen katalyseres ved anvendelse af kobber ved forhøjet temperatur, men lavere end 250 ° C..
applikationer
opløsningsmiddel
Ethylacetat anvendes som opløsningsmiddel og fortyndingsmiddel, der anvendes til rengøring af printplader. Den anvendes som et opløsningsmiddel ved fremstillingen af det modificerede humleekstrakt og ved koffeinaffaldet af kaffe og te blade. Den bruges i trykfarverne til markering af frugt og grøntsager.
Ethylacetat anvendes som tekstilindustri som rengøringsmiddel. Det bruges til kalibrering af termometre, der anvendes til adskillelse af sukkerarter. I malingsindustrien anvendes det som opløsningsmiddel og fortyndingsmiddel af de anvendte materialer.
Kunstige smagsstoffer
Det bruges til udarbejdelse af frugt smag; For eksempel: banan, pære, fersken og ananas, samt drue aroma mv..
analytisk
Det anvendes til bestemmelse af vismut, bor, guld, molybdæn og platin samt thalliumopløsningsmiddel. Ethylacetat har evnen til at ekstrahere mange forbindelser og elementer til stede i vandig opløsning, såsom: fosfor, kobolt, wolfram og arsen.
Organiske synteser
Ethylacetat anvendes i industrien som et viskositetsreduktionsmiddel til harpikser, der anvendes i fotoresistformuleringer. Det anvendes til fremstilling af acetamid, acetylacetat og methylheptanon.
kromatografi
I laboratorierne anvendes ethylacetat som mobil fase af søjlekromatografi og som ekstraktionsopløsningsmiddel. Ved at have ethylacetatet et relativt lavt kogepunkt er det let at fordampe, hvilket gør det muligt at koncentrere de opløste stoffer i opløsningsmidlet.
entomologi
Ethylacetat anvendes i entomologi til kvælende insekter placeret i en beholder, hvilket gør det muligt at indsamle og studere. Dampene af ethylacetat dræber insektet uden at ødelægge det og forhindre dets hærdning, hvilket letter samlingen til opsamling.
risici
-LD50 af ethylacetat hos rotter indikerer en lav toksicitet. Det kan dog irritere hud, øjne, hud, næse og hals.
-Eksponering for høje niveauer kan forårsage svimmelhed og besvimelse. Langtidseksponering kan også påvirke lever og nyre.
-Indånding af ethylacetat i en koncentration på 20.000 - 43.000 ppm kan forårsage lungeødem og blødning.
-Grænseværdien for erhvervsmæssig eksponering er fastsat af OSHA ved 400 ppm i luften i gennemsnit under et arbejdstidsarbejde på 8 timer.
referencer
- Steven A. Hardinger. (2017). Illustreret ordliste for organisk kemi: ethylacetat (EtOAc). Hentet fra: chem.ucla.edu
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10th udgave.). Wiley Plus.
- Morrison, R.T. og Boyd, R.N. (1990). Organisk kemi (5ta udgave). Redaktionel Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Ethylacetat. Hentet fra: en.wikipedia.org
- Bomuld S. (s.f.). Ethylacetat. Hentet fra: chm.bris.ac.uk
- Pubchem. (2019). Ethylacetat. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Anvendelser og anvendelser af ethylacetat. Hentet fra: foodweeteners.com
- New Jersey Department of Health of Senior Services. (2002). Ethylacetat. [PDF]. Hentet fra: nj.gov


