Sodium chloride (NaCl) struktur, egenskaber, anvendelser, toksicitet
den natriumchlorid, også kaldet almindeligt salt eller bordssalt, er et binært uorganisk salt af alkalimetallnatrium og halogenchlorinet. Det er den største bestanddel af spiseligt salt, og dets mineralform er kendt som halit. Dens molekylære formel er NaCl og beskriver det støkiometriske forhold for dets ioner (Na+ cl-) og ikke for et diskret molekyle (Na-Cl)
Natriumchlorid er et hvidt krystallinsk faststof, der er dannet ved kombinationen af natrium, sølvhvide metal, som reagerer voldsomt med vand, og elementet chlor, en giftig, ætsende og bleg grøn gas.

I det øvre billede vises en del af NaCl-krystaller. Hvordan er det muligt, at to elementer så farlige som Na og Cl2, Kan et spiseligt salt dannes? For det første er den kemiske ligning for dens dannelse:
2Na (s) + Cl2(g) => 2NaCl (s)
Svaret ligger i karakteren af forbindelsen i NaCl. At være ionisk, egenskaberne af Na+ og Cl- de er diagonalt forskellige fra de af deres neutrale atomer.
Natrium er et vigtigt element, men i sin ioniske form. Na+ er den vigtigste ekstracellulære kation med en koncentration på ca. 140 mEq / lt, og sammen med dets ledsagende anioner, Cl- og HCO3- (bicarbonat), er primært ansvarlige for værdien af osmolaritet og ekstracellulært volumen.
Desuden er Na+ er ansvarlig for genereringen og ledningen af nerveimpulser i neuronale axoner, samt at initiere muskelkontraktion.
NaCl har været brugt siden oldtiden til smag mad og for at bevare kød, på grund af sin evne til at dræbe bakterier og forhindre nedbrydning.
Det er også nødvendigt for fremstilling af natriumhydroxid (NaOH) og molekylært chlor (Cl2) ved omsætning af NaCl med vandet under hydrolyse:
2H2O (1) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
I katoden (-) akkumuleres H2 (g) og NaOH. I mellemtiden ophobes Cl ved anoden (+)2 (G). Natriumhydroxid anvendes til fremstilling af sæbe og klor til fremstilling af PVC-plast.
indeks
- 1 Struktur af natriumchlorid
- 1.1 ensartet celle
- 2 Egenskaber
- 2.1 Molekylformel
- 2,2 molekylvægt
- 2.3 Fysisk beskrivelse
- 2,4 farve
- 2,5 Smag
- 2,6 kogepunkt
- 2,7 smeltepunkt
- 2,8 Opløselighed i vand
- 2.9 Opløselighed i organiske opløsningsmidler
- 2,10 Densitet
- 2.11 Damptryk
- 2.12 Stabilitet
- 2.13 Nedbrydning
- 2,14 Viskositet
- 2.15 Korrosion
- 2,16 pH
- 3 anvendelser
- 3.1 i mad
- 3.2 Industrielle anvendelser
- 3.3 derhjemme
- 3.4 Andre anvendelser
- 3.5 Terapeutiske anvendelser
- 4 Toksicitet
- 4.1 Indtagelse
- 4.2 Irritation og fysisk kontakt
- 5 referencer
Struktur af natriumchlorid
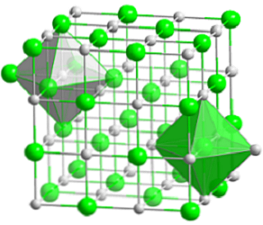
Den kompakte kubiske struktur af natriumchlorid er repræsenteret i det øvre billede. De voluminøse grønne kugler svarer til Cl anioner-, mens hvide, til Na kationer+. Bemærk, hvordan NaCl krystal består af et netværk af ioner arrangeret ved deres elektrostatiske interaktioner i et 1: 1 forhold.
Selv om stænger er vist i billedet, er bindingerne ikke kovalente, men ioniske. Anvendelsen af stængerne er nyttig, når koordinationsgeometrien vises omkring en ion. For eksempel i tilfælde af NaCl hver Na+ er omgivet af seks kl- (hvid oktaedron), og hver Cl- af seks Na+ (grøn oktaedron).
Derfor har den en koordinering (6,6), hvis tal angiver, hvor mange naboer der omgiver hver ion. Tallet til højre angiver naboerne af Na+, mens den ene til venstre, Cl-.
Andre repræsentationer udelade anvendelsen af stænger at fremhæve de oktaedriske huller med den struktur, som det interstitielle rum mellem seks anioner Cl- (eller Na kationer+) pakket. Dette arrangement observeres i andre mono (MX) eller polyatomiske uorganiske salte og kaldes perlesalt..
Unitary celle
Stentsaltets enhedscelle er kubisk, men hvilke terninger repræsenterer det præcist i billedet ovenfor? Oktaedronerne giver svaret. Begge dækker i alt fire små terninger.
Disse terninger har dele af ionerne i deres hjørner, kanter og ansigter. Observation af omhyggeligt en ion Na+ den er placeret i midten og tolv af dem i kanterne. En ion på den ene kant kan deles af fire terninger. Så der er 4 Na ioner+ (12 × 1/4 + 1 = 4).
For Cl ioner-, otte er placeret i hjørnerne og seks i kanterne. Da de ioner, der er placeret ved hjørnerne, deler plads med otte andre terninger og ved kanterne med seks, har de 4 Cl ioner- (8 × 1/8 + 6 × 1/2 = 4).
Det foregående resultat fortolkes som følger: i NaCl-enhedscellen er der fire Na-kationer+ og fire Cl anioner-; andel, der svarer til den kemiske formel (a Na+ for hver Cl-).
egenskaber
Molekylformel
NaCl.
Molekylvægt
58,44 g / mol.
Fysisk beskrivelse
Et krystallinsk faststof.
farve
Transparente farveløse krystaller eller hvidt krystallinsk pulver.
smag
salt.
Kogepunkt
2,575 ºF til 760 mmHg.
1.465 ºC.
Smeltepunkt
1.474 ºF (800,7 ºC).
Både kogepunktet og smeltepunktet afspejler den varme, der er nødvendig for at overvinde den krystallinske retikulære energi. Derfor bekræfter disse målinger den ioniske karakter af NaCl.
Opløselighed i vand
Større end eller lig med 100 mg / ml ved 68 ° F.
36,0 g / 100 ml ved 25 ºC.
Det er faktisk et hygroskopisk salt, der bevarer fugt fra miljøet.
Opløselighed i organiske opløsningsmidler
0,065 g / 100 ml ethanol ved 25 ° C; 10 g / 100 g glycerol ved 25 ° C; 2,15 g / 100 ml flydende ammonium ved 40 ° C; 1,4 g / 100 ml methanol ved 25 ° C; 7,15 g / 100 ethylenglycol ved 25 ° C og 5,21 g / 100 g myresyre ved 25 ° C.
tæthed
2.165 g / cm3 ved 77 ºC.
Damptryk
1 mmHg til 1.589 ºF.
stabilitet
Den er stabil under de anbefalede opbevaringsforhold.
nedbrydning
Ved opvarmning til høje temperaturer nedbryder det udledning af dampe af saltsyre og dinatriumoxid.
viskositet
Viskositet af mættede opløsninger 1,93 mPa-s.
korrosion
Det er ætsende for mange metaller.
pH
6,7 til 7,3 i vandig opløsning.
applikationer
I mad
-Natriumchlorid er blevet brugt siden oldtiden for at forbedre smag af mad og dets bevarelse. Saltet af kødet er en måde at bevare den mod bakteriehandling, da det forsinker proteinafbrydelsen.
-På den anden side, salt øger osmolariteten omkring kød, som forårsager absorption ved osmose vand bakterier, der forårsager deletion.
Industrielle anvendelser
Fødevareindustrien
-I fødevareindustrien anvendes salt som en smagsforstærker, fermenteringskontroladditiv, teksturstyringsmiddel og farveudvikler. For eksempel tilsættes salt for at fremhæve farve i bacon, skinke og andre kødprodukter.
-Salt tjener som et bindemiddel til fremstilling af pølser. Det bidrager til dannelsen af en bindemiddelgel bestående af kød, fedt og fugt.
-Ved forarbejdning af mel til brødfremstilling tilsættes salt under tilberedning for at kontrollere fermenteringshastigheden for brøddejen. Det bruges også til at styrke gluten og som smagsforstærker samt en påfyldning af bagværk.
-Det bruges til fremstilling af morgenmadsprodukter, blandet eller tilberedt mel, pommes frites, måltider til hunde og katte mv..
Syntese af kemiske produkter
-Natriumchlorid anvendes som råmateriale til fremstilling af natriumhydroxid og chlor, hvilket igen er nyttigt i mange kemiske industrier.
-Salt anvendes til forarbejdning af forskellige metaller, for eksempel aluminium, kobber, stål og vanadium. Det anvendes også til fremstilling af natriumchlorat, som efterfølgende anvendes i syntesen af klordioxid, en oxygenbaseret blegemiddel. Klordioxid er mindre skadeligt for miljøet end andre blegemidler.
I læderindustrien
-Salt bruges til at hæmme bakterieaktiviteten inde i skindene, såvel som at hjælpe med dens rehydrering.
I tekstilindustrien
-Salt bruges som en mordant i farvning af stoffer. Det bruges som en saltvandskskylning for at fjerne organiske forureninger og for at skabe en positiv ladning på overfladen af stofferne, der tillader forening af de negativt ladede farvestoffer.
I olieindustrien
-Ved olie- og gasudforskning er salt en vigtig bestanddel af brøndborevæsker. Det bruges til at flokkulere og forøge densiteten af borevæske, således at overvinde de højt tryk gasbrønde, der skal opnås. Derudover opretholder saltet mætningen af borevæsken.
-Saltet hjælper med at komprimere jorden, hvor veje er bygget. Reducerer forskydningen forårsaget i undergrunden ved ændringer i luftfugtighed og biltrafik.
Derhjemme
Saltet er blevet brugt ved gnidning i rengøring af overflader, gryder og pander. Også i forebyggelse af skimmelsvamp og som pletfjerner. Det bruges også i mange mærker af shampoo og tandpasta.
Andre anvendelser
På vejene
-I afventning af snefald er vejene dækket af saltlage, som forhindrer forening af is til overfladen af vejen. Til optøning anvendes en blanding af saltvand og salt, og andre kemiske komponenter såsom magnesium eller calciumchlorider tilsættes nogle gange. Brugen af salt og saltvand er ikke effektiv ved temperaturer under -10ºC.
Ved tilføjelse af en dråbe salt cryoscopic punkt, en kolligative egenskab af opløsningerne og derved hæmmer noget isdannelse forekommer.
-På grund af sin hygroskopiske tilstand anvendes saltet som et billigt tørremiddel.
I harpikserne anvendes til vandblødgøring
Hårdt vand indeholder calcium- og magnesiumioner, der forhindrer sæbevirkningen og producerer aflejringer af alkaliske materialer i forskellige udstyr og rør. Ved vandblødgøring anvendes ionbytterharpikser. Salt anvendes til fremstilling og regenerering af harpikser.
Ildslukkere
Natriumklorid anvendes i ildslukkere til bekæmpelse af brande, hvor brændbare metaller er til stede, såsom magnesium-, kalium-, natrium- og NK-legeringer.
Saltet fungerer som en kølelegeme og også som en knuser, der begrænser adgangen til ilt til ild.
I brillerne
Natriumchloridkrystaller anvendes i optiske komponenter som vinduer og prismer, især til infrarødt lys. Men da saltet er meget hygroskopisk, opstår der en slags frost, der dækker linserne. Af denne grund er natriumkloridlinser blevet erstattet af zink selenid (ZnSe).
Terapeutiske anvendelser
At supplere manglen på salte i kroppen
-Når der er en udbrydning af kroppen af Na+, skal udskiftes for at opretholde ekstracellulær osmolaritet, nervedannelse og muskelkontraktion.
-NaCl anvendes til behandling og forebyggelse af mangel på natrium og chlor, som skyldes overdreven sved under eksponering for høje temperaturer. Det bruges også i overdreven diurese eller overdreven begrænsning af saltindtag.
-Parenteral afgivelse af en 045% NaCl-opløsning anvendes til behandling af hyperosmolær diabetes. Det opfylder en rehydrerende funktion og tjener til at vurdere status for nyrefunktionen.
-Injektioner af hypertoniske opløsninger med en NaCl-koncentration på mere end 0,9% vægt / volumen,
-De bruges, når der er en alvorlig udtømning af Na+, at være en restaurering af den essentielle ion. Denne hyponatremi kan være konsekvensen af en behandling med frie elektrolytter eller med en koncentration af Na+.
Hyponatremi kan også skyldes overdreven vandindtagelse, ikke kontrolleret af utilstrækkelig nyrefunktion.
Ved behandlinger og ukonventionelle anvendelser
-NaCl-inhalationsopløsninger anvendes til at fortynde de lægemidler, der anvendes under nebuliseringsprocessen. Det bruges også til tracheal vask og kunstvanding. 0,9% saltopløsning anvendt i næsesprayer.
-20% NaCl-opløsninger anvendes til intra-amniotisk transabdominal installation, hvilket fremkalder en sen abort i graviditetens anden trimester.
-Natriumchlorid kan anvendes som lokal antiseptisk middel. Takket være dens osmotiske kapacitet er det i stand til at dehydrere et bredt spektrum af vira og bakterier i en uforbrændt tilstand; Derfor bruges den som en smertefuld antiseptisk til at desinficere sår.
toksicitet
indtagelse
Det har kun en sundhedsskadelig virkning, hvis indtaget er højt og i lang tid. Under disse omstændigheder ville hypernatremi forekomme med den deraf følgende stigning i ekstracellulært volumen, der ville føre til højt blodtryk.
Irritation og fysisk kontakt
Det har kun en toksisk virkning, hvis indåndingen er meget høj. Ved kontakt med huden i overdreven form kan det forårsage tørhed. Endelig forårsager det en øjeblikkelig irritation ved kontakt med øjnene.
referencer
- Shiver & Atkins. (2008). Uorganisk kemi (Fjerde udgave, s. 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Kemi. (8. udgave). CENGAGE Learning, s. 482-483.
- Natriumchlorid (2018). Natriumchlorid: Fordele, anvendelser, egenskaber, risici. Modtaget fra: clorurodesodio.org
- Pubchem. (2018). Natriumchlorid. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Natriumchlorid. Hentet fra: en.wikipedia.org
- Amerikanske elementer. (2018). Natriumchlorid. Modtaget fra: americanelements.com


