Biologisk katalysator ydeevne og eksempler
en biologisk katalysator eller biokatalysator er et molekyle, som generelt er proteinbaseret, og som har kapacitet til at fremskynde de kemiske reaktioner, der forekommer i levende væsener. Katalysatorproteinmolekyler er enzymer, og de af RNA-natur er ribozymer. I denne artikel vil vi fokusere på at udforske enzymer, som er de bedst kendte biologiske katalysatorer.
I mangel af enzymer kan det enorme antal reaktioner, der finder sted i cellen, og det tillader livet, ikke kunne forekomme. Disse er ansvarlige for at fremskynde processen i størrelsesorden tæt på 106 - og i nogle tilfælde meget større.
indeks
- 1 katalyse
- 2 enzymer
- 2.1 Hvad er et enzym?
- 2.2 Karakteristika for enzymer
- 2.3 Nomenklatur og klassificering af enzymer
- 2.4 Hvordan enzymer virker?
- 2,5 Enzymatiske hæmmere
- 2.6 Eksempler
- 3 Forskel mellem biologiske katalysatorer (enzymer) og kemiske katalysatorer
- 3.1 Reaktioner katalyseret af enzymer forekommer hurtigere
- 3.2 De fleste enzymer arbejder under fysiologiske forhold
- 3.3 Specificitet
- 3.4 Enzymatisk regulering er nøjagtig
- 4 referencer
katalyse
En katalysator er et molekyle, som er i stand til at ændre hastigheden af en kemisk reaktion uden at blive forbrugt i nævnte reaktion.
Kemiske reaktioner involverer energi: de indledende molekyler involveret i reaktionen eller reaktanterne begynder med en grad af energi. En yderligere mængde energi absorberes for at nå "overgangsstatus". Derefter frigives energien med produkterne.
Energiforskellen mellem reaktanterne og produkterne udtrykkes som ΔG. Hvis energieniveauerne af produkterne er større end reaktanterne, er reaktionen endergonisk og ikke spontan. I modsætning hertil, hvis produktets energi er lavere, er reaktionen exergonisk og spontan.
Men hvis en reaktion er spontan, betyder det ikke, at det vil ske med en mærkbar hastighed. Reaktionshastigheden afhænger af ΔG * (stjernen refererer til aktiveringsenergien).
Læseren skal holde disse begreber i tankerne for at forstå, hvordan enzymerne fungerer.
enzymer
Hvad er et enzym?
Enzymer er biologiske molekyler af utrolig kompleksitet, der hovedsagelig består af proteiner. Proteiner er igen lange kæder af aminosyrer.
Et af de mest fremragende egenskaber ved enzymer er deres specificitet i målmolekylet - dette molekyle kaldes substratet.
Karakteristik af enzymer
Enzymer findes i flere former. Nogle er helt sammensat af proteiner, mens andre har ikke-proteinregioner kaldet cofactors (metaller, ioner, organiske molekyler osv.).
Således er et apoenzym et enzym uden dets cofaktor, og kombinationen af apoenzymet og dets cofaktor kaldes et holoenzym.
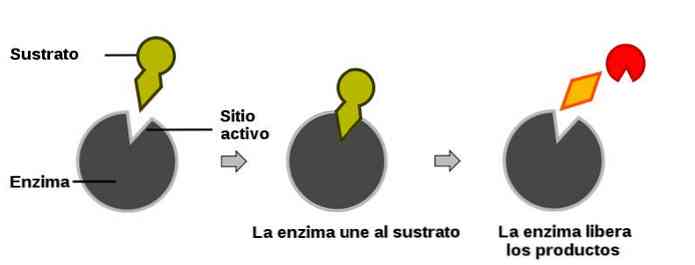
De er molekyler af en betydeligt stor størrelse. Imidlertid deltager kun et lille sted af enzymet direkte i reaktionen med substratet, og denne region er det aktive sted.
Når reaktionen begynder, er enzymet koblet med dets substrat som en nøgle er forbundet med dens lås (denne model er en forenkling af den faktiske biologiske proces, men tjener til at illustrere processen).
Alle kemiske reaktioner, der forekommer i vores krop, katalyseres af enzymer. Faktisk, hvis disse molekyler ikke eksisterede, skulle vi vente hundreder eller tusinder af år for reaktionerne at fuldføre. Derfor skal reguleringen af enzymatisk aktivitet styres på en meget specifik måde.
Nomenklatur og klassificering af enzymer
Når vi ser et molekyle, hvis navn slutter i -ase, kan vi være sikre på, at det er et enzym (selv om der er undtagelser fra denne regel, såsom trypsin). Dette er konventionen til at betegne enzymernes navn.
Der er seks grundlæggende typer af enzymer: oxidoreduktaser, transferaser, hydrolaser, lyaser, isomeraser og ligaser; ansvarlig for: redox reaktioner, overførsel af atomer, hydrolyse, tilsætning af dobbeltbindinger, isomerisering og binding af molekyler.
Hvordan enzymer virker?
I afsnittet om katalyse nævnte vi, at reaktionshastigheden afhænger af værdien af ΔG *. Jo højere denne værdi er, jo langsommere og langsommere reaktionen. Enzymet er ansvarlig for at reducere den nævnte parameter - hvilket øger reaktionshastigheden.
Forskellen mellem produkterne og reaktanterne forbliver identiske (enzymet påvirker ikke det), ligesom fordeling af det samme. Enzymet letter dannelsen af overgangstilstanden.
Enzyminhibitorer
I forbindelse med undersøgelsen af enzymer er inhibitorer stoffer, som formår at reducere katalysatorens aktivitet. De er klassificeret i to typer: konkurrencedygtige og ikke-konkurrencedygtige hæmmere. De af den første type konkurrerer med substratet og de andre gør det ikke.
Generelt er inhiberingsprocessen reversibel, selv om nogle inhibitorer kan forblive koblet til enzymet næsten permanent.
eksempler
Der er en stor mængde enzymer i vores celler - og i cellerne i alle levende væsener. Imidlertid er de mest kendte dem, der deltager i metaboliske veje, såsom glycolyse, Krebs-cyklus, elektron transportkæde, blandt andre..
Succinatdehydrogenase er et enzym af oxidoreduktase-typen, der katalyserer oxidationen af succinat. I dette tilfælde involverer reaktionen tabet af to hydrogenatomer.
Forskel mellem biologiske katalysatorer (enzymer) og kemiske katalysatorer
Der er katalysatorer af en kemisk natur, som, ligesom de biologiske, øger reaktionshastigheden. Der er dog bemærkelsesværdige forskelle mellem begge typer af molekyler.
Enzymkatalyserede reaktioner forekommer hurtigere
For det første formår enzymerne at øge reaktionshastigheden i størrelsesordener tæt på 106 op til 1012. Kemiske katalysatorer øger også hastigheden, men kun få ordrer.
De fleste enzymer arbejder under fysiologiske forhold
Da de biologiske reaktioner udføres inden for levende væsener, omgiver de deres optimale forhold de fysiologiske værdier af temperatur og pH. Kemikere har derimod brug for drastiske betingelser for temperatur, tryk og surhed.
specificitet
Enzymer er meget specifikke i de reaktioner, de katalyserer. I de fleste tilfælde arbejder de kun med et substrat eller med få. Specificiteten gælder også for den type produkter, de producerer. Udvalget af substrater af kemiske katalysatorer er meget bredere.
De kræfter, der bestemmer specificiteten af interaktionen mellem enzymet og dets substrat, er de samme som dikterer konformationen af det samme protein (Van der Waals-interaktioner, elektrostatiske, hydrogenbindinger og hydrofobiske).
Den enzymatiske regulering er præcis
Endelig har enzymerne større reguleringskapacitet, og aktiviteten af disse varierer alt efter koncentrationen af forskellige stoffer i cellen.
Blandt de regulerende mekanismer finder vi allosterisk kontrol, den kovalente modifikation af enzymerne og variationen i mængden af enzym, der syntetiseres.
referencer
- Berg, J. M., Stryer, L., & Tymoczko, J. L. (2007). biokemi. Jeg vendte om.
- Campbell, M. K. & Farrell, S. O. (2011). Biokemi. Sjette udgave. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Lærebog om biokemi. John Wiley & Sons.
- Koolman, J., & Röhm, K. H. (2005). Biokemi: tekst og atlas. Ed. Panamericana Medical.
- Mougios, V. (2006). Udøve biokemi. Human Kinetics.
- Müller-Esterl, W. (2008). Biokemi. Grundlag for medicin og biovidenskab. Jeg vendte om.
- Poortmans, J.R. (2004). Principper for motion biokemi. Karger.
- Voet, D., & Voet, J. G. (2006). biokemi. Ed. Panamericana Medical.


