Cyclohexen struktur, egenskaber, syntese og anvendelser
den cydohexen er en alken eller cyklisk olefin, hvis molekylære formel er C6H10. Den består af en farveløs væske, uopløselig i vand og blandbar med mange organiske opløsningsmidler. Den er karakteriseret ved at være brandfarlig, og i naturen findes den sædvanligvis i kul tjære..
Cyklohexen syntetiseres ved delvis hydrogenering af benzen og ved dehydrering af alkoholcyclohexanol; det vil sige en mere rusten form. Ligesom andre cycloalkener undergår det reaktioner af elektrofiltilsætning og med frie radikaler; for eksempel halogeneringsreaktionen.

Dette cykliske alken (topbillede) danner azeotrope blandinger (ikke adskilles ved destillation), med lavere alkoholer og eddikesyre. Det er ikke meget stabilt i længere tids opbevaring, da det nedbrydes under påvirkning af sollys og ultraviolet stråling.
Cyclohexen anvendes som et opløsningsmiddel og har derfor mange anvendelser, såsom: stabilisator af højoktangasoliner og til udvinding af olier.
Men det vigtigste er, at cyclohexen tjener som et mellemprodukt og råmateriale til fremstilling af mange nyttige forbindelser, blandt dem: cyclohexanon, adipinsyre, maleinsyre, cyclohexan, butadien, cyclohexylcarboxylsyre osv..
indeks
- 1 Struktur af cyclohexen
- 1.1 Intermolekylære interaktioner
- 2 Egenskaber
- 2.1 Kemiske navne
- 2,2 molekylvægt
- 2.3 Fysisk udseende
- 2.4 lugte
- 2,5 kogepunkt
- 2.6 Smeltepunkt
- 2.7 Flammepunkt
- 2,8 Opløselighed i vand
- 2.9 Opløselighed i organiske opløsningsmidler
- 2,10 Densitet
- 2.11 Damptæthed
- 2.12 Damptryk
- 2.13 Selvantændelse
- 2.14 Nedbrydning
- 2,15 Viskositet
- 2.16 Forbrændingsvarme
- 2.17 Fordampningsvarme
- 2.18 Overfladespænding
- 2,19 Polymerisering
- 2.20 Lugtgrænsen
- 2.21 Brekningsindeks
- 2,22 pH
- 2,23 Stabilitet
- 2.24 Reaktioner
- 3 Sammenfatning
- 4 anvendelser
- 5 risici
- 6 referencer
Opbygning af cyclohexen
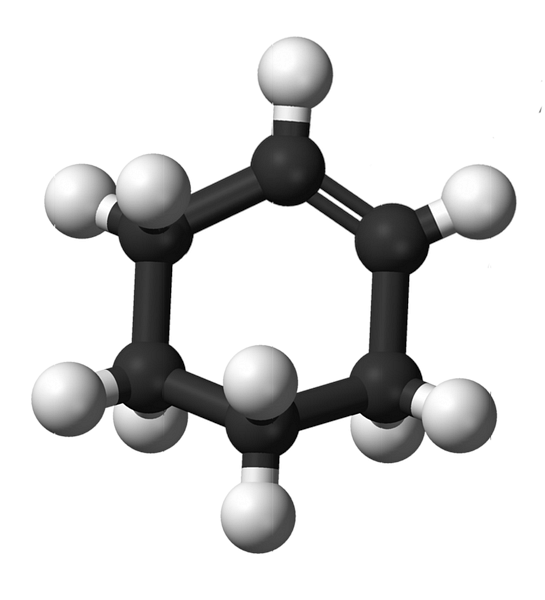
Opbygningen af cyclohexen med en model af kugler og søjler er vist i billedet ovenfor. Man kan bemærke de seks carbonring og dobbeltbindingen, begge umættelser af forbindelsen. Fra dette perspektiv ser det ud til, at ringen er flad; men det er slet ikke.
For startere har carbonerne i dobbeltbindingen sp hybridisering2, som giver dem en trigonal plan geometri. Derfor er disse to carbonatomer, og dem der støder op til dem, i samme plan; mens de to carbonatomer i den modsatte ende (til dobbeltbindingen) er over og under det nævnte plan.
Det nederste billede illustrerer perfekt, hvad der netop er blevet forklaret.

Bemærk at det sorte bånd er sammensat af fire carbonatomer: de to af dobbeltbindingen og de andre der støder op til dem. Det udsatte perspektiv er det, der ville opnås, hvis en tilskuer placerede sit øje lige foran dobbeltbindingen. Det kan ses, at et kulstof er over og under dette plan.
Da cyclohexenmolekylet ikke er statisk, vil de to carbonater udveksle: en vil sænke, mens den anden vil stige over flyet. Så du ville forvente, at molekylet opfører sig.
Intermolekylære interaktioner
Cyclohexen er et carbonhydrid, og derfor er dets intermolekylære interaktioner baseret på dispersionskræfterne i London.
Dette skyldes, at molekylet er apolært, uden permanent dipolmoment, og dets molekylvægt er den faktor der bidrager mest til at holde den sammenhængende i væsken.
Også dobbeltbindingen øger graden af interaktion, da den ikke kan bevæge sig med samme fleksibilitet som for de andre carboner, og dette favoriserer vekselvirkningen mellem nabo molekyler. Det er af denne grund, at cyclohexen har et lidt højere kogepunkt (83 ° C) end cyclohexan (81 ° C).
egenskaber
Kemiske betegnelser
Cyclohexen, tetrahydrobenzen.
Molekylvægt
82.146 g / mol.
Fysisk udseende
Farveløs væske.
lugt
Sød lugt.
Kogepunkt
83 ºC til 760 mmHg.
Smeltepunkt
-103,5 ºC.
Antændelsespunkt
-7ºC (lukket kop).
Opløselighed i vand
Næsten uopløselig (213 mg / l).
Opløselighed i organiske opløsningsmidler
Blandbar med ethanol, benzen, carbontetrachlorid, petroleumsether og acetone. Det forventes, at det vil være i stand til at opløse apolære forbindelser, ligesom nogle af allotropene af kul.
tæthed
0,810 g / cm3 ved 20ºC.
Damptæthed
2,8 (i forhold til luften er lig med 1).
Damptryk
89 mmHg ved 25ºC.
Selvantændelse
244 ºC.
nedbrydning
Nedbrydes i nærværelse af uran salte under påvirkning af sollys og ultraviolet stråling.
viskositet
0,625 mPascal ved 25 ºC.
Forbrændingsvarme
3,751,7 kJ / mol ved 25ºC.
Fordampningsvarme
30,46 kJ / mol ved 25 ºC.
Overfladespænding
26,26 mN / m.
polymerisation
Det kan polymerisere under visse forhold.
Lugtgrænsen
0,6 mg / m3.
Brydningsindeks
1,4465 ved 20 ºC.
pH
7-8 ved 20ºC.
stabilitet
Cyclohexen er ikke særlig stabil under langtidsopbevaring. Eksponering for lys og luft kan forårsage produktion af peroxider. Ligeledes er det uforeneligt med stærke oxidationsmidler.
reaktioner
-Cycloalkener oplever primært additionsreaktioner, både elektrofile og frie radikaler.
-Reagerer med brom til dannelse af 1,2-dibromcyclohexan.
-Oxiderer hurtigt i nærvær af kaliumpermanganat (KMnO4).
-Det er i stand til at fremstille et epoxid (cyclohexenoxid) i nærværelse af peroxybenzoesyre.
syntese
Cyclohexen fremstilles ved syrekatalyse af cyclohexanol:

Symbolet A repræsenterer den varme, der er nødvendig for at fremme udgangen af OH-gruppen som et vandmolekyle i surt medium (-OH2+).
Cyclohexen fremstilles også ved delvis hydrogenering af benzen; det vil sige to af sine dobbeltbindinger tilføjer et hydrogenmolekyle:

Selvom reaktionen synes simpel, kræver det store tryk på H2 og katalysatorer.
applikationer
-Det har anvendelighed som et organisk opløsningsmiddel. Derudover er det et råmateriale til fremstilling af adipinsyre, adipicaldehyd, maleinsyre, cyclohexan og cyclohexylcarboxylsyre.
-Det anvendes til fremstilling af cyclohexanchlorid, en forbindelse, der anvendes som mellemproducent i fremstillingen af farmaceutiske produkter og gummitilsætningsstoffer..
-Cyclohexen anvendes også i syntese af cyclohexanon, råmateriale til fremstilling af lægemidler, pesticider, parfume og farvestoffer.
-Cyclohexen er involveret i syntesen af aminocyclohexanol, en forbindelse, som anvendes som et overfladeaktivt middel og emulgeringsmiddel..
-Desuden kan cyclohexen anvendes til fremstilling i butadien laboratoriet. Sidstnævnte forbindelse anvendes til fremstilling af syntetisk gummi til fremstilling af dæk til biler og anvendes også til fremstilling af akrylplast.
-Cyclohexen er det råmateriale til syntese af lysin, phenol, polycycloolefinharpiks og gummiadditiver.
-Det bruges som stabilisator af højoktan gasoliner.
-Involveret i syntesen af vandtætte belægninger, sprængfaste film og bindende bindemidler til belægninger.
risici
Cyclohexen er ikke en meget giftig forbindelse, men det kan forårsage rødme af hud og øjne ved kontakt. Dens indånding kan producere hoste og døsighed. Desuden kan indtagelse forårsage døsighed, vejrtrækningsbesvær og kvalme.
Cyklohexen absorberes dårligt i mavetarmkanalen, så der forventes ingen alvorlige systemiske virkninger på grund af indtagelse. Den største komplikation er dets aspiration af åndedrætssystemet, som kan producere kemisk lungebetændelse.
referencer
- Joseph F. Chiang, og Simon Harvey Bauer. (1968). Molekylær struktur af cyclohexen. J. Am. Chem. Soc. 1969, 91, 8, 1898-1901.
- Karry Barnes. (2019). Cyclohexen: Fare, Syntese & Struktur. Undersøgelse. Hentet fra: study.com
- Morrison, R.T. og Boyd, R.N. (1987). Organisk kemi (5ta Edition.). Redaktionel Addison-Wesley Iberoamericana.
- Pubchem. (2019). Cyclohexen. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Kemisk bog. (2019). Cyclohexen. Hentet fra: chemicalbook.com
- Toksikologiske datanetværk. (2017). Cyclohexen. TOXNET. Hentet fra: toxnet.nlm.nih.gov
- Chemoxy. (N.D.). Strukturen for cyclohexen er. Hentet fra: chemoxy.com


