Ethyletheregenskaber, struktur, opnåelse, anvendelser
den ethylether, også kendt som diethylether, er en organisk forbindelse, hvis kemiske formel er C4H10O. Det er karakteriseret ved at være en farveløs og flygtig væske, og derfor skal flaskerne holdes lukkede så hermetisk som muligt.
Denne ether er klassificeret som et medlem af dialkylethere; det vil sige, de har formlen ROR ', hvor R og R' repræsenterer forskellige kulsegmenter. Og som det beskriver dens mellemnavn, diethylether, er to radikaler-ethyl dem, der binder til oxygenatomet.

Oprindeligt blev ethylether anvendt som en generel bedøvelse, introduceret i 1846 af William Thomas Green Morton. På grund af dets antændelighed blev dens anvendelse imidlertid afvist, idet den erstattedes med andre mindre farlige anæstetika..
Denne forbindelse er også blevet brugt til at estimere tidspunktet for blodcirkulationen under bedømmelsen af patienternes kardiovaskulære status.
Inden for kroppen kan diethylether omdannes til kuldioxid og metabolitter; sidstnævnte bliver udskilt i urinen. Imidlertid udåndes det meste af den indgivne ether i lungerne uden at undergå nogen ændring.
På den anden side anvendes det som opløsningsmiddel til sæber, olier, parfumer, alkaloider og tandkød.
indeks
- 1 Struktur af ethylether
- 1.1 Intermolekylære kræfter
- 2 Fysiske og kemiske egenskaber
- 2.1 Andre navne
- 2,2 Molekylformel
- 2,3 Molekylvægt
- 2.4 Fysisk udseende
- 2,5 lugt
- 2.6 Smag
- 2,7 kogepunkt
- 2,8 smeltepunkt
- 2.9 Flammepunkt
- 2.10 Opløselighed i vand
- 2.11 Opløselighed i andre væsker
- 2,12 Tæthed
- 2.13 Damptæthed
- 2.14 Damptryk
- 2,15 Stabilitet
- 2.16 Selvantændelse
- 2.17 Nedbrydning
- 2,18 Viskositet
- 2.19 Forbrændingsvarme
- 2.20 Fordampningsvarme
- 2.21 Overfladespænding
- 2.22 ioniseringspotentiale
- 2.23 Lugtgrænsen
- 2.24 brydningsindeks
- 3 Indhentning
- 3.1 Fra ethylalkohol
- 3.2 Fra ethylen
- 4 Toksicitet
- 5 anvendelser
- 5.1 Organisk opløsningsmiddel
- 5.2 Generel anæstesi
- 5.3 ether af etheren
- 5.4 Evaluering af blodcirkulationen
- 5.5 Undervisningslaboratorier
- 6 referencer
Struktur af ethylether
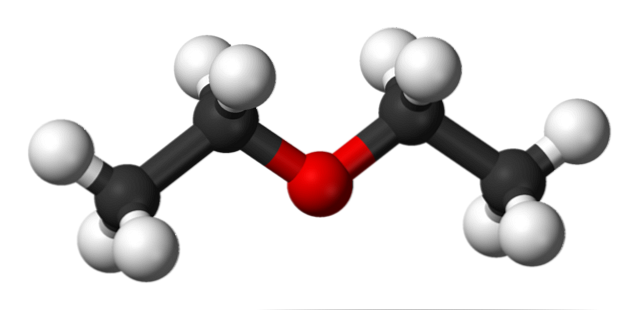
I billedet ovenfor har vi en repræsentation med en model af kugler og stænger af ethyletherens molekylære struktur.
Som det kan ses, har den røde kugle, der svarer til oxygenatomet, to ethylgrupper forbundet på begge sider. Alle links er enkle, fleksible og frit drejelige omkring akserne σ.
Disse rotationer stammer fra stereoisomerer kendt som konformatorer; at mere end isomerer, de er alternative rumlige tilstande. Strukturen af billedet svarer nøjagtigt til anti-konformeren, hvor alle dets atomgrupper er forskudt (adskilt fra hinanden).
Hvad ville være den anden konformator? Den formørkede, og selvom dit billede ikke er tilgængeligt, visualiserer du det med en U-form. Ved de øvre ender af U ville du finde methylgrupperne, -CH3, som ville opleve steriske frastødninger (de ville kollidere i rummet).
Det forventes derfor, at CH-molekylet3CH2OCH2CH3 Adopter anti-konformationen det meste af tiden.
Intermolekylære kræfter
Ved hvilke intermolekylære kræfter reguleres molekylerne af ethylether i væskefasen? De opretholdes i væsken hovedsagelig takket være dispersionskræfterne, da deres dipolmoment (1,5D) mangler en region, der er tilstrækkeligt mangelfuld i elektronisk densitet (δ +)
Dette skyldes, at intet carbonatom i ethylgrupperne giver for meget elektrontæthed til oxygenatomet. Ovenstående er tydeligt med kortet over elektrostatisk potentiale af ethylether ved hånden (bundbillede). Bemærk fraværet af en blå region.
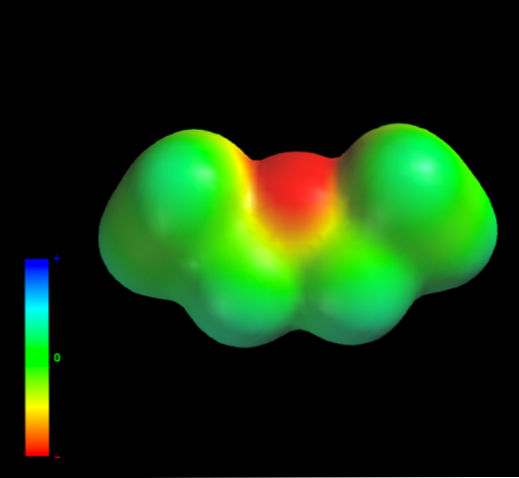
Oxygen kan heller ikke danne hydrogenbindinger igen, fordi der ikke er tilgængelige O-H-bindinger i den molekylære struktur. Derfor er det de øjeblikkelige dipoler og deres molekylmasse, der favoriserer deres spredningskræfter.
På trods af dette er det meget opløseligt i vand. Hvorfor? Fordi dets oxygenatom med en højere elektrontæthed kan acceptere hydrogenbindinger fra et vandmolekyle:
(CH3CH2)2Oδ- - δ+H-OH
Disse vekselvirkninger er ansvarlige for 6,04 g af denne ether, der opløses i 100 ml vand.
Fysiske og kemiske egenskaber
Andre navne
-Diethylether
-ethoxyethan
-Ethyloxid
Molekylformel
C4H10O eller (C2H5)2O.
Molekylvægt
74,14 g / mol.
Fysisk udseende
Farveløs væske.
lugt
Sød og krydret.
smag
Brændende og sødt.
Kogepunkt
94,3 ºF (34,6 ºC) til 760 mmHg.
Smeltepunkt
-177,3 ºF (-116,3 ªC). Stabile krystaller.
Antændelsespunkt
-49ºF (lukket beholder).
Opløselighed i vand
6,04 g / 100 ml ved 25 ºC.
Opløselighed i andre væsker
Blandbar med kortkædede alifatiske alkoholer, benzen, chloroform, petroleumsether, fedtopløsningsmiddel, mange olier og koncentreret saltsyre.
Opløseligt i acetone og meget opløseligt i ethanol. Det er også opløseligt i naphtha, benzen og olier.
tæthed
0,714 mg / ml ved 68 ªF (20 ºC).
Damptæthed
2,55 (i forhold til luft taget med densitet 1).
Damptryk
442 mmHg ved 68ºF. 538 mmHg ved 25 ° C. 58,6 kPa ved 20 ºC.
stabilitet
Det oxideres langsomt ved hjælp af luft, fugt og lys med dannelsen af peroxider.
Dannelsen af peroxider kan forekomme i æterbeholdere, der er blevet åbnet, og som forbliver i opbevaring i mere end seks måneder. Peroxider kan detonere ved friktion, slag eller opvarmning.
Undgå kontakt med: zink, halogener, ikke-metalliske oxyhalider, stærke oxidationsmidler, chromylchlorid, tementinolier, nitrater og metalchlorider.
Automatisk tænding
356ºF (180ºC).
nedbrydning
Når det opvarmes opløses det og udsender en skarp og irriterende røg.
viskositet
0,2444 cPoise ved 20 ºC.
Forbrændingsvarme
8.807 Kcal / g.
Fordampningsvarme
89,8 cal / g ved 30 ºC.
Overfladespænding
17.06 dyn / cm ved 20º C.
Ioniseringspotentiale
9,53 eV.
Lugtgrænsen
0,83 ppm (renhed er ikke angivet).
Brydningsindeks
1.355 ved 15 ºC.
opnå
Fra ethylalkohol
Ethylether kan opnås ud fra ethylalkohol, i nærvær af svovlsyre som en katalysator. Svovlsyren i et vandigt medium dissocierer fremstilling af hydroniumionen, H3O+.
Den vandfri ethylalkohol strømmer gennem svovlsyreopløsningen opvarmet mellem 130 ° C og 140 ° C, hvilket fremkalder protonationen af ethylalkoholmolekyler. Efterfølgende reagerer et andet molekyle ikke-protoneret ethylalkohol med det protonerede molekyle.
Når dette sker, fremmer det nukleofile angreb af det andet molekyle af ethylalkohol frigivelsen af vand fra det første molekyle (den protonerede); som et resultat dannes en protoneret ethylether (CH3CH2OHCH2CH3), med delvist ladet oxygen positiv.
Imidlertid mister denne syntesemetode effektivitet, fordi svovlsyren fortyndes med det vand, der fremstilles under processen (produkt af dehydrering af ethylalkohol).
Reaktionstemperaturen er kritisk. Ved temperaturer under 130 ° C er reaktionen langsom, og for det meste destilleres ethylalkohol.
Over 150 ° C forårsager svovlsyre dannelsen af ethylen (dobbeltbindingen alken) i stedet for at kombinere med ethylalkohol for at danne ethylether.
Fra ethylen
I den modsatte proces, dvs. hydrering af ethylen i dampfasen, kan ethylether dannes som et biprodukt ud over ethylalkohol. Faktisk producerer denne syntetiske vej det meste af denne organiske forbindelse.
Denne proces anvender phosphorsyrekatalysatorer fastgjort til en fast bærer, idet de er i stand til at justere for at producere mere ether.
Dehydrering i dampfase af ethanol i nærvær af aluminiumoxidkatalysatorer kan give et udbytte på 95% ved fremstilling af ethylether.
toksicitet
Det kan forårsage irritation på huden og øjnene ved kontakt. Kontakt med huden kan forårsage tørring og revner. Eteren trænger normalt ikke ind i huden, da den hurtigt fordampes.
Øjenirritationen forårsaget af æteren er normalt mild, og i tilfælde af alvorlig irritation er skaden sædvanligvis reversibel.
Dens indtagelse giver narkotiske virkninger og irritation i maven. Alvorlig indtagelse kan forårsage nyreskade.
Indånding af æteren kan forårsage irritation af næse og hals. I tilfælde af indånding af ether kan forekomme: døsighed, spænding, svimmelhed, opkastning, uregelmæssig vejrtrækning og øget spytning.
Høj eksponering kan forårsage tab af bevidsthed og endda død.
OSHA fastlægger en erhvervsmæssig eksponeringsgrænse på 800 ppm i gennemsnit under en 8-timers skift.
Niveauer af øjenirritation: 100 ppm (human). Niveauer af øjenirritation: 1200 mg / m3 (400 ppm).
applikationer
Organisk opløsningsmiddel
Det er et organisk opløsningsmiddel, der bruges til at opløse brom, jod og andre halogener; Størstedelen af lipider (fedtstoffer), harpikser, rene gummier, nogle alkaloider, tandkød, parfumer, celluloseacetat, cellulose nitrat, carbonhydrider og farvestoffer.
Derudover anvendes den til udvinding af de aktive principper for animalske væv og planter, fordi det har en lavere densitet end vand og flyder på den, hvilket efterlader de ønskede stoffer opløst i etheren.
Generel anæstesi
Det er blevet brugt som en generel bedøvelse siden 1840, erstatning af chloroform for at have en terapeutisk fordel. Det er imidlertid et brændbart stof, og derfor oplever alvorlige vanskeligheder for dets anvendelse inden for kliniske rammer.
Derudover producerer det hos patienter nogle uønskede postoperative bivirkninger såsom kvalme og opkastning.
Af disse årsager er anvendelsen af ether som generel bedøvelse blevet kasseret, idet den erstattes af andre anæstetika, såsom halothan..
Etherens ånd
Etheren blandet med ethanol blev anvendt til dannelse af opløsningen kaldet etherand, anvendt til behandling af gastrisk flatulens og mildere former for gastralgi.
Vurdering af blodcirkulationen
Ether er blevet brugt til at evaluere blodcirkulationen mellem en arm og lungerne. Etheren injiceres i en arm og bringer blodet til højre atrium og derefter til højre ventrikel og derfra til lungerne.
Den tid, der går fra injektionen af etheren til optagelse af etherlugt i udåndet luft, er ca. 4 til 6 s.
Undervisningslaboratorier
Ether bruges i undervisningslaboratorier i mange eksperimenter; for eksempel i demonstration af Mendel's genetiske love.
Eteren er vant til at dæmpe fluerne i slægten Drosophila og tillade de nødvendige krydsninger mellem dem for at bevise lovene om genetik
referencer
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10th udgave.). Wiley Plus.
- Carey F. (2008). Organisk kemi (Sjette udgave). Mc Graw Hill.
- The Sevier. (2018). Diethylether. Science Direct. Hentet fra: sciencedirect.com
- Editors of Encyclopaedia Britannica. (2018). Ethylether. Britannica ncyclopædia. Hentet fra: britannica.com
- PubChem (2018). Ether. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Diethylether. Hentet fra: en.wikipedia.org
- Sikkerhedsark XI: ethylether. [PDF]. Gendannet fra: quimica.unam.mx


